
| A. | 该反应属于置换反应 | |
| B. | 该反应属于离子反应 | |
| C. | 若有0.1mol氯气参与反应,则转移电子0.1mol | |
| D. | 该反应中Cl2既是氧化剂又是还原剂 |
分析 A、2Fe2++Cl2═2Fe3++2Cl-,是化合反应;
B、是氧化还原的离子反应;
C、1mol氯气参与反应,转移2mol的电子;
D、氯气中氯的化合价降低是氧化剂.
解答 解:A、2Fe2++Cl2═2Fe3++2Cl-,是化合反应,而不是置换反应,故A错误;
B、有离子参加的氧化还原反应,所以是氧化还原的离子反应,故B正确;
C、1mol氯气参与反应,转移2mol的电子,所以有0.1mol氯气参与反应,则转移电子0.2mol,故C错误;
D、氯气中氯的化合价降低是氧化剂,只是氧化剂,故D错误;
故选B.
点评 本题考查氧还原反应的概念和电子数目的转移,侧重于基础知识的考查,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 明矾水解形成的Al(OH)3胶体能杀菌消毒,可用于水的净化 | |
| B. | 镀锡的铁制品比镀锌的铁制品耐腐蚀 | |
| C. | pH=6的某溶液一定呈酸性 | |
| D. | 二次电池充电时,电池上标有“+”的电极应与外接电源的正极相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 容器 | 温度/K | 物质的起始浓度(mol/L) | 物质的平衡浓度(mol/L) | |||
| CO2(g) | H2(g) | C2H5OH(g) | H2O(g) | C2H5OH(g) | ||
| 甲 | 500 | 0.20 | 0.60 | 0 | 0 | 0.083 |
| 乙 | 500 | 0.40 | 1.20 | 0 | 0 | |
| 丙 | 600 | 0 | 0 | 0.10 | 0.30 | 0.039 |
| A. | 该反应正反应为吸热反应 | |
| B. | 达平衡时,容器甲中的逆反应速率比容器乙中的小 | |
| C. | 达平衡时,转化率:α(CO2,甲)+α(C2H5OH,丙)>1 | |
| D. | 达平衡时,甲、乙容器内:2c(CO2,甲)<c(CO2,乙) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 2015年8月12日,天津滨海新区发生特大爆炸事故,原因是仓库里存放了大量的硝酸铵、氰化钠、电石和金属钠等危险化学品.下列有关叙述正确的是( )
2015年8月12日,天津滨海新区发生特大爆炸事故,原因是仓库里存放了大量的硝酸铵、氰化钠、电石和金属钠等危险化学品.下列有关叙述正确的是( )| A. | 金属钠可以保存在石蜡油中,并贴上右图标识 | |
| B. | 硝酸铵、氰化钠、电石和金属钠均属于电解质 | |
| C. | 危险化学品危害人类健康,应禁止生产 | |
| D. | 可以用大量水扑灭爆炸现场的大火 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该物质既能与强酸反应又能与强碱反应 | |
| B. | 该物质是Al(OH)3和Na2CO3的混合物 | |
| C. | 1 mol[NaAl(OH)2CO3]最多可消耗4 mol H+ | |
| D. | 该药剂不适合于胃溃疡患者服用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
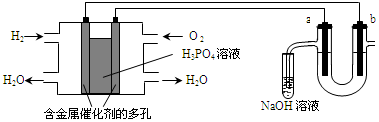 用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a,b为石墨电极).下列说法中正确的是( )
用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a,b为石墨电极).下列说法中正确的是( )| A. | 电池工作时,正极反应式为O2+2H2O+4e-═4OH | |
| B. | 电解时,电子流动路径是负极→外电路→阴极→溶液→阳极→正极 | |
| C. | 试管中NaOH溶液用来吸收电解时产生的Cl2 | |
| D. | 当电池中消耗2.24L(标准情况下)H2时,b极周围会产生0.021mol气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NaCl溶液一定不能发生丁达尔效应 | |
| B. | 将1L2mol•-1FeCl3溶液制成胶体后,其中含有2NA个氢氧化铁胶粒(NA为阿伏加德罗常数值) | |
| C. | FeCl3溶液与Fe(OH)3胶体的本质区别是有无丁达尔效应 | |
| D. | 可吸入颗粒(如硅酸盐粉尘)形成气溶胶(分散剂为气体的胶体),对人体健康危害极大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用淘米水浇花 | |
| B. | 农田普及滴灌技术 | |
| C. | 未及时修复破损的供水管道 | |
| D. | 工业废水经处理后作为城市绿化用水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol甲烷和1mol氯气在光照条件下充分反应,生成1mol CH3Cl | |
| B. | 等物质的量的乙烯与碳酸二甲酯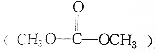 完全燃烧耗氧量相同 完全燃烧耗氧量相同 | |
| C. | 苯和液溴在FeCl3的催化作用下发生加成反应 | |
| D. | 苯在工业上可通过石油分馏得到 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com