
某温度下,向体积为2L的密闭容器中加入CH3OH,发生反应
2CHOH(g)
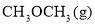 +H2O(g)
+H2O(g) 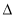 H=-25 kJ·mol
H=-25 kJ·mol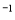 ,反应过程中测定的部分数据见下表。
,反应过程中测定的部分数据见下表。
已知该温度下反应的平衡常数K=400,下列说法正确的是
反应时间/min |
|
|
0 | 2.05 | 0 |
| 0.6 | |
| 0.05 |
A.反应在t2 min时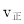 ≠
≠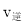
B.反应达到平衡时,放出的热量为50 kJ
C.反应在t1 min内的平均速率为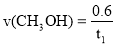 mol·L
mol·L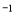 ·min
·min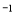
D.若反应达到平衡后,缩小容器体积,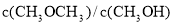 变大
变大
科目:高中化学 来源:2014-2015四川省邛崃市高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列各组离子中,在碱性溶液中能大量共存,且溶液为无色透明的是
A.K+ MnO4- Cl- SO42- B.Na+ AlO2- Cl- SO42-
C.SO42- Na+ HCO3- Ba2+ D.Na+ NO3- NH4+ SO42-
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省宜春市高二下学期第一次月考化学试卷(解析版) 题型:填空题
有机化合物A、B分子式不同,它们只可能含碳、氢、氧元素中的两种或三种.如果将A、B不论以何种比例混和,只要其物质的量之和不变,完全燃烧时所消耗的氧气和生成的水的物质的量也不变.那么,A、B组成必须满足的条件是 ; .若A是甲烷,则符合上述条件的化合物B中,分子量最小的是(写出分子式) ,并写出分子量最小的含有甲基的B的2种同分异构体结构简式: , 。
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省宜春市高二下学期第一次月考化学试卷(解析版) 题型:选择题
为把溴水中溴单质萃取出来,下列物质可达到目的的是
A.乙醇 B.苯酚溶液 C.直馏汽油 D.乙酸
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市东城区高三综合能力测试二理综化学试卷(解析版) 题型:实验题
(15分)实验小组同学看到一则报道:某造纸厂误将槽车中漂白液(NaCl和NaClO的混合液)倒入盛放饱和KAl(SO4)2溶液的池中,造成中毒事件。该小组同学为探究中毒原因进行了如下实验。
(1)小组同学依据漂白液具有漂白消毒的性质推测,漂白液中ClO-具有氧化性。实验如下:
Ⅰ.用pH试纸检验,漂白液pH>7,饱和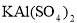 溶液pH<7。
溶液pH<7。
Ⅱ.取10 mL漂白液,依次加入Na2SO3溶液和BaCl2溶液,有白色沉淀生成,经检验白色沉淀不溶于盐酸。
Ⅲ.另取10 mL,漂白液,加入品红溶液,溶液红色逐渐变浅,一段时间后褪为无色。
Ⅳ.再取10 mL漂白液,加入品红溶液,加入少量稀硫酸酸化后,溶液红色立即变为无色。
①漂白液pH大于7的原因是(用离子方程式表示)__________。
②由实验Ⅱ得出ClO-具有氧化性,写出反应的离子方程式__________。
③对比实验Ⅲ和Ⅳ说明ClO-氧化性与溶液酸碱性的关系是__________。
(2)小组同学依据(1)中的实验,提出:漂白液在酸性溶液中有Cl2生成。用下图所示的装置继续实验,探究漂白液在酸性溶液中是否能反应生成Cl2。
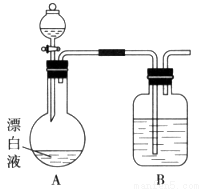
①装置B的作用是__________;盛放的药品是__________。
②若打开分液漏斗活塞向烧瓶中加入硫酸,不久烧瓶中有黄绿色气体产生。A中反应的离子方程式__________。
③若打开分液漏斗活塞向烧瓶中加入饱和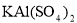 溶液,首先观察到产生大量的白色胶状沉淀,不久烧瓶中有黄绿色气体产生。A中加
溶液,首先观察到产生大量的白色胶状沉淀,不久烧瓶中有黄绿色气体产生。A中加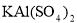 溶液反应的离子方程式是__________。
溶液反应的离子方程式是__________。
(3)上述实验说明漂白液与酸性溶液混合会产生Cl2。若取10 mL漂白液与足量BaCl2溶液混合后,不断通入SO2至过量,在实验过程中可能的实验现象是__________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市东城区高三综合能力测试二理综化学试卷(解析版) 题型:选择题
下列标志的高分子材料的单体,其中一种单体与其他三种单体均不是同系物的是

查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省台州市高二下学期第一次月考化学试卷(解析版) 题型:填空题
(6分)(1)1mol某烃A与1mol H2起反应生成1mol乙苯,该加成反应的化学方程式为:
_________________________________________________________;
烃A发生加聚反应的化学方程式为____________________________________;
(2)写出60℃时1,3—丁二烯与溴1:1反应的方程式_________________________
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省台州市高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列分子中的所有碳原子均在同一条直线上的是:
A.CH3CH2CH2CH3
B.CH3 — CH=CHCH3
C.HC≡C—CH2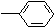
D.CH3—C≡C—C≡C—CH3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省安庆市高三第二次模拟考试理综化学试卷(解析版) 题型:填空题
用湿法制磷酸副产品氟硅酸(H2SiF6 )生产无水氟化氢的工艺如下图所示:
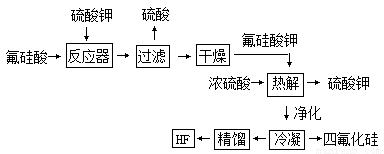
已知:氟硅酸钾(K2SiF6)微酸性,有吸湿性,微溶于水,不溶于醇。在热水中水解成氟化钾、氟化氢及硅酸。
(1)写出反应器中的化学方程式:
(2)在实验室过滤操作中所用的玻璃仪器有: ;
在洗涤氟硅酸钾(K2SiF6)时常用酒精洗涤,其目的是: ;
(3)该流程中哪些物质可以循环使用: (用化学式表达)
(4)氟化氢可以腐蚀刻画玻璃,在刻蚀玻璃过程中也会生成H2SiF6 ,试写出该反应方程式: ;
(5)为了测定无水氟化氢的纯度,取标况下的气体产物2.24L,测得质量为3.1g,并将气体通入含足量的Ca(OH)2 溶液中,得到5.85gCaF2沉淀,则无水氢氟酸质量分数为: 。(保留2位有效数字)通过计算结果,试解释,为什么标况下2.24L产物的质量远远大于2.0g, 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com