
A.H2S 2H+ + S2- 2H+ + S2- | B.HClO = H+ +ClO- |
C.CH3COONH4 NH4+ +CH3COO- NH4+ +CH3COO- | D.HCO3—+H2O  H3O++CO32- H3O++CO32- |
科目:高中化学 来源:不详 题型:单选题
| A.常温下物质的量浓度相等①NH4HSO4、②(NH4)2SO4、③(NH4)2CO3三种溶液中c(NH4+) ①<②<③ |
| B.在纯水中加入少量硫酸或硫酸铵,均可抑制水的电离 |
| C.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 |
| D.常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.浓氨水 | B.纯水 |
| C.少量K2CO3固体 | D.少量浓H2SO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
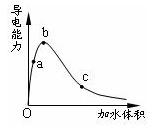
| A.a、b、c三点溶液的pH:c<a<b |
| B.a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:c<a<b |
| C.a、b、c三点中b点n(H+)最大 |
| D.a、b、c三点醋酸的电离程度:a<b<c |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 电离度
电离度 的数值,其实验方案可设计如下:
的数值,其实验方案可设计如下: __________。
__________。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com