
为了验证木炭可被浓H2SO4氧化成CO2,选用下图所示仪器(内含物质)组装成实验装置:

(1)如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):
接 , 接 , 接 ;
(2)仪器乙、丙应有怎样的实验现象才表明已检验出CO2?
乙中 ____ ,丙中 ______ ;
(3)丁中酸性KMnO4溶液的作用是 ;
(4)写出甲中反应的化学方程式 。
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源:2013-2014广东省第一学期期终考试高一级化学科试卷甲卷(解析版) 题型:选择题
下列反应的离子方程式错误的是
A.碘水加到溴化钠溶液中:2 Br- + I2 === 2I- + Br2
B.氯气通入碘化钾溶液中:2I- + Cl2=== 2Cl- + I2
C.氯气溶于水:Cl2 + H2O === 2H+ + Cl-+ ClO-
D.硝酸银溶液中滴加碘化钠溶液:Ag+ + I- === AgI↓
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省深圳市高考预测理综化学试卷(解析版) 题型:选择题
X、Y、Z、W是元素周期表前四周期中的常见元素。其相关信息如下表:
元素 | 相关信息 |
X | X的一种核素的质量数为14,中子数为8 |
Y | Y与X同周期,且它的一种氧化物只能用排水法收集 |
Z | Z的单质常温下为黄绿色气体 |
W | W的原子核外电子总数是其电子层数的4倍 |
下列说法正确的是
A.原子半径:W> X>Y,离子半径:W>Z
B.氧化物对应的水化物的酸性:Z> Y>X
C.Y的最高正价含氧酸,可由它的氢化物为原料来制取
D.W的单质与X的一种氧化物不能发生置换反应
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省江门市高二调研测试理综化学试卷(解析版) 题型:填空题
3,5—二甲氧基苯酚是重要的有机合成中间体,其合成反应如下:

该反应后的混合物含有:3,5—二甲氧基苯酚、甲醇、水和HCl。
已知:甲醇、乙醚和3,5—二甲氧基苯酚的部分物理性质如下表:
物质 | 沸点/℃ | 熔点/℃ | 密度(20℃)/(g/cm3) | 溶解性 |
甲醇 | 64.7 | — | 0.7915 | 易溶于水 |
乙醚 | 34.5 | — | 0.7138 | 难溶于水 |
3,5—二甲氧基苯酚 | 172 | 36 | — | 易溶于甲醇、乙醚, 微溶于水 |
现在实验室对反应后的混合物进行分离提纯:
(1)利用与其它物质 差异较大的特点,可先用蒸馏法分离出甲醇,蒸馏操作时使用的玻璃仪器有:酒精灯、 、温度计、冷凝管 、接引管、锥形瓶。
(2)①蒸馏出甲醇后,加入乙醚进行 、 操作,有机层在分液漏斗的 层。
②双项选择:选用乙醚这种试剂的主要原因是( )
A.乙醚易挥发
B.3,5—二甲氧基苯酚在乙醚中溶解度大于在水中的溶解度
C.乙醚难溶于水
D.3,5—二甲氧基苯酚熔点较低
(3)经上述步骤分离得到的有机层再用饱和NaHCO3溶液洗涤,其目的是 。
(4)洗涤完成后,加入无水CaCl2干燥,过滤除去干燥剂,蒸馏除去乙醚,得到固体产物,为进一步提纯固体产物还要进行 操作。
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省江门市高二调研测试理综化学试卷(解析版) 题型:选择题
在25℃的条件下,下列叙述正确的是
A.将稀氨水逐滴加入稀硫酸中,当溶液的pH=7时,c(SO )= c(NH4+)
)= c(NH4+)
B.pH=3的醋酸溶液,稀释至原体积的10倍后pH=4
C.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,溶液pH<7
D.向0.1mol·L-1的氨水中加入少量硫酸铵固体,则溶液中c(OH-) 增大
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省梅州市高一下学期期中化学试卷(解析版) 题型:选择题
短周期元素甲,乙,丙,丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第VA族,甲和丙同主族,丁原子最外层电子数和电子层数相等,则 ( )
A.原子半径:丙>丁>乙
B.单质的还原性:丁>丙>甲
C.甲,乙,丙的氧化物均为共价化和物
D.乙,丙,丁的最高价氧化物对应的水化物能相互反应
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省梅州市高一下学期期中化学试卷(解析版) 题型:选择题
下列叙述中错误的是 ( )
A.原子半径:Cl>S>O B.还原性:Na>Mg>Al
C.稳定性:HF>HCl>HBr D. 酸性:HClO4>H2SO4>H3PO4
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省惠州市高一下学期期末考试化学(理)试卷(解析版) 题型:实验题
某小组同学用下图装置进行实验研究(a、b、c表示止水夹).请评价或完善其方案:
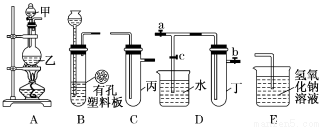
将装置A、C、E相连接,用MnO2和浓盐酸制取氯气,请回答:
①.氯元素在周期表中的位置为 。
②.A中反应的离子方程式:___ _。
③.E中氢氧化钠溶液的作用__________ 。
在C中加入适量的水可制得氯水.将所得氯水分成两份进行实验,其操作、现象和结论为:
实验序号 | 实验操作 | 现象 | 结论 |
Ⅰ | 将氯水滴入品红溶液 | 品红溶液褪色 | 氯气有漂白性 |
Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气与水反应的产物具有酸性 |
④.实验Ⅰ推出的相应结论是否合理? _________,若不合理,请说明理由(若合理,无需填写)________________________________ ______________。
⑤.实验Ⅱ推出相应的结论是否合理?_________,若不合理,请说明理由(若合理,无需填写)____________________________________ ____________________。
(2) 为比较Cl2和I2的氧化性强弱,将A、C、E相连, C中盛的试剂可以为___ _ __。
(3) 将B、D、E相连,在B中装浓硝酸和铜片,可制得NO2并进行有关实验.
①.B中反应的化学方程式_____________________ ______ __________。
②.先若关闭c,当丁中充满红棕色的NO2时,再关闭止水夹a、b ,微热试管丁, 丁中可观察到的实验现象 。
查看答案和解析>>
科目:高中化学 来源:2013-2014广东省惠州市高一下学期期末考试化学(理)试卷(解析版) 题型:选择题
下列氢氧化物中,碱性最强的是
A. KOH B. NaOH C.Mg(OH)2 D. Al(OH)3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com