
����Ŀ��
ʹ��̪��죬����֮���ת����ϵ����ͼ����ʾ��
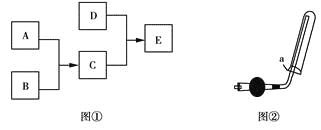
��1��������B��ȼ���ѵ�������ʢ������A�ļ���ƿ����Ӧ�����е�ʵ�������� ������ţ�
������ ������ɫ��ȥ ��ƿ���а��� ��ƿ���а���
������ȼ�գ�������ɫ���� ������ȼ�գ�������ɫ����
��2��ʵ������D�Ļ�ѧ����ʽΪ ��
��3��ʵ���ҿ�������ͼ����ʾװ���ռ�D������������ȷ���� ������ţ���
��D���岻������ˮ���ռ�
���������ʢ�м�ʯ��
��ͼ���е�aΪ���ţ��������Ƿ�ֹ�����ݳ�
��4������D�������Ļ�ѧ����ʽΪ ��
��5������E�Ļ�ѧʽ�� ��E���������ʷ��������������������� ������ţ���
������ʣ������������������������ǵ���ʣ�����
���𰸡���1���٢ڢۢ�
��2��Ca(OH)2+2NH4Cl![]() CaCl2+H2O +2NH3��
CaCl2+H2O +2NH3��
��3�� �٢�
��4��4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
��5��NH4Cl �٢ڢܢ�
�����������������AΪ����ɫ��D��������ˮ����A��������D�ǰ�����A��B��C��DΪ���壬��B��������C���Ȼ������壬����E���Ȼ�李�
��1�������������а�����ȼ�գ������ɫ������ɫ����ȥ��ƿ���а������Ȼ�������������е�Сˮ�ν�ϣ����֣�ȼ�շ�Ӧ���Ƿ��ȷ�Ӧ������ѡ�٢ڢۢ���
��2��ʵ�����ư����Ļ�ѧ����ʽΪCa(OH)2+2NH4Cl![]() CaCl2+H2O +2NH3����
CaCl2+H2O +2NH3����
��3��������������ˮ����������ˮ���ռ�����������ˮ�Լ��ԣ����ü�ʯ�Ҹ��ͼ���е�aӦΪʪ���ɫʯ����ֽ�����鰱���Ƿ��ռ��������Դ�ѡ�٢���
��4�����������������Ļ�ѧ����ʽΪ4NH3+5O2![]() 4NO+6H2O��
4NO+6H2O��
��5��E���Ȼ�泥���ѧʽΪNH4Cl�����ǻ�����Ǵ�������Σ��ǵ���ʣ����Դ�ѡ�٢ڢܢ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����25����1.01��105Pa�£���22gCO2ͨ�뵽750mL 1.0 mol��L��1��NaOH��Һ�г�ַ�Ӧ���ų�x kJ�������ڸ�������1molCO2ͨ�뵽2L 1.0 mol��L��1��NaOH��Һ�г�ַ�Ӧ���ų�ykJ��������CO2��NaOH��Ӧ����NaHCO3���Ȼ�ѧ��Ӧ����ʽΪ] ( )
A. CO2(g) + NaOH(aq)=NaHCO3(aq) ��H����(2y��x) kJ��mol��1
B. CO2(g) + NaOH(aq)=NaHCO3(aq) ��H����(4x��y) kJ��mol��1
C. CO2(g) + NaOH(aq)=NaHCO3(aq) ��H����(2x��y) kJ��mol��1
D. CO2(g) + NaOH(aq)=NaHCO3(aq) ��H����(8x��2y) kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��T��ʱ�������Ϊ0.5L�����������ܱ������з������淴Ӧ��
2A��g����B��g��![]() 2C��g����H����QkJ/mol��Q��0��
2C��g����H����QkJ/mol��Q��0��
ʵ���÷�Ӧ����ʼ���ﵽƽ��ʱ���й��������±���
������� | ��ʼʱ���������ʵ���/mol | �ﵽƽ��ʱ��ϵ�����ı仯 | ||
A | B | C | ||
�� | 2 | 1 | 0 | 0.75Q kJ |
�� | 0.4 | 0.2 | 1.6 | |
����������ȷ����
A�������������з�Ӧ��ƽ�ⳣ����Ϊ36
B���������з�Ӧ�ﵽƽ��ʱ�ų�������Ϊ0.05 Q kJ
C������������ͨ�뺤����ƽ��ʱA��ת���ʲ���
D�������������䣬�����������ֺ��ݾ��ȣ���ﵽƽ��ʱC���������С��2/3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ָ�����з�Ӧ��SiO2�����ֵĻ�ѧ���ʻ����ã���A��Eѡ����ѡ����ȷ�����������ڡ�
��SiO2��2NaOH===Na2SiO3��H2O
��SiO2��2C===Si��2CO��
��SiO2��3C===SiC��2CO��
��SiO2��4HF===SiF4����2H2O
a����Ϊ�����ijɷֱ����Ķ�ʹ��������ʴ
b��������
c�������������ͨ��
d��δ�μ�������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��С������������һ���ƽ�������С����ͨ��ʵ����֤ʵ��������Dz�����ͭп�Ͻ��Ƴɵķ���Ʒ��������ѡ�õ��Լ��ǣ�������
A.MgCl2
B.H2SO4
C.AgNO3
D.CuSO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֤�������к��е��۵��Լ���
A�����ۣ��⻯����ֽ B��������Һ C����ˮ D���⻯��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£��ֱ��Ը�����ء�����ء���������Ϊԭ����ȡ���������Ƶ�ͬ��ͬѹ����ͬ���������ʱ��������Ӧ��ת�Ƶĵ�����֮��Ϊ�� ��
A��1��1��2 B��2��2��1 C��2��3��1 D��4��3��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ճ������Լ����������Ź㷺�����á����й��ڽ�����˵������ȷ���ǣ�������
A.�Ͻ����������ɷֽ��������ʲ���ȫ��ͬ
B.��ҵ�Ͻ���Mg��Al�����õ�����ڵ��Ȼ����Ƶõ�
C.����ұ���ı����ǽ��������ӵõ����ӱ�ɽ���ԭ��
D.Խ���õĽ���Խ��ұ����ұ����������������й�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭп�Ͻ��ƳɵĻ�ͭ��Ʒ��������Ϊ�ǻƽ����з����в�����������α���ǣ�������
A.�۲����
B.����������
C.�ⶨ�ܶ�
D.��������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com