
��1����ijҩƷ����ԼΪ32g����������ƽȷ�������������á���ʾ�����̷������룬�á���ʾ������ȡ�£������б���Ŀո��ڣ��á��͡���ʾ��Ӧ����ķ��ϻ�ȡ�£�
50g0g0g0g-5g
----
��ͼ��ʾ������500mL 1.5mol/L Na2CO3��Һ������Na2CO3������Ϊ����g��
ʵ��������Ⱥ�˳��Ϊ���������ţ���
��3��������һ�����ʵ���Ũ�ȵ���Һʱ���á�ƫ�ߡ�ƫ�͡���Ӱ�족��ʾ���в�����������ҺŨ�ȵ�Ӱ�죮
������ͲȡҺ̬���ʣ�����ʱ��������Ͳ����������Һ��Ũ��������
������450mL 0.1mol•L﹣1��NaOH��Һ����������ƽ��ȡNaOH����1.8g������
������NaOH��Һʱ���������õ�NaOH�������С�ձ����ܽ⣬δ����ȴ����ת�Ƶ�����ƿ�в�����������
�ܶ���ʱ���ӿ̶���������
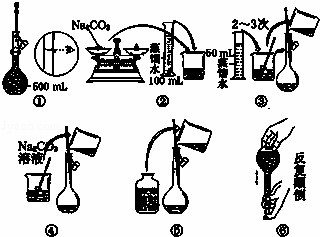
���㣺-����һ�����ʵ���Ũ�ȵ���Һ��
������-��1�������ȼ�����������룬�ٻ�С���룬���ʹ�������ԭ����ɣ�
����500mL 1.5mol/L Na2CO3��Һ���е�̼���Ƶ����ʵ��������̼���Ƶ���������������һ�����ʵ���Ũ�ȵ���Һ�IJ����������
��3������ʵ�������c=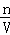 ������Ӱ����з�����
������Ӱ����з�����
���-�⣺��1��ijҩƷ����ԼΪ32g����������ƽȷ�����������������̼���50g���룬��������ʾΪ��50g������Ȼ��20g���룬�����������㣬��ʾΪ��20g�����ټ�20g���룬20g������������ʾΪ����������10g���룬10g�����������㣬��ʾΪ��10g�����ټ�5g���룬5g����������������5g���룬��ʾΪ��5g����������ƶ����뵽2g���е�ƽ���ʴ�Ϊ�� ��
��
����500mL 1.5mol/L Na2CO3��Һ����Ҫ0.75mol̼���ƣ�����Ϊ��106g/mol��0.75mol=79.5g��
����һ�����ʵ���Ũ�ȵ���Һ�IJ���Ϊ�����㡢�������ܽ⡢��ȴ��ת�ơ�ϴ�ӡ����ݡ�ҡ�ȵȣ�����ʵ��ʱͼ����ʾ�������Ⱥ�˳��Ϊ���ڢܢۢݢ٢ޣ��ʴ�Ϊ��79.5���ڢܢۢݢ٢ޣ�
��3��������ͲȡҺ̬���ʣ�����ʱ������Ͳ��ʹ����ȡҺ�����������ֵС��ʹ��������Һ��Ũ��ƫ�ͣ��ʴ�Ϊ��ƫ�ͣ�
������û��450mL�������ƿ������ѡ��500mL����ƿ����������������Ƶ����ʵ���n=CV=0.5L��0.1mol/L=0.05mol������m=nM=0.05mol��40g/mol=2.0g������������ƽ��ȡ�������ƹ���1.8g���Ƴ�����Һ��Ũ��ƫ�ͣ��ʴ�Ϊ��ƫ�ͣ�
��δ����ȴ����ת�Ƶ�����ƿ�в����ݣ���Һ���ƫС��Ũ��ƫ�ߣ��ʴ�Ϊ��ƫ�ߣ�
�ܶ���ʱ���ӿ̶��ߣ���Һ���ƫ��Ũ��ƫ�ͣ��ʴ�Ϊ��ƫ�ͣ�
������-���⿼��������һ�����ʵ���Ũ�ȵ���Һ���輰����������Ŀ�ѶȲ���ע��������������һ�����ʵ���Ũ�ȵ���Һ�ķ�����������������ķ����ͼ��ɣ�
��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��Ӧ X������+Y������⇌2Z������+Q��Q��0������һ�������£���Ӧ��Y��ת�����뷴Ӧʱ�䣨t���Ĺ�ϵ��ͼ��ʾ����ʹ����a��Ϊ����b�ɲ�ȡ�Ĵ�ʩ�ǣ���
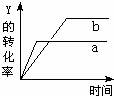
A�� ������� B�� �����¶� C�� ����ѹǿ D�� ����Y��Ũ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и��仯������ԭ��صķ�Ӧ���ǣ�������
| �� | A�� | �ڿ����н���������Ѹ�������γɱ����� |
| �� | B�� | �Ӻ�ˮ��ͨ����ѧ�����õ�����þ |
| �� | C�� | ���ȵ���˿����ˮ�Ӵ��������������ɫ������ |
| �� | D�� | п��ϡ���ᷴӦʱ������������CuSO4��Һ��ʹ��Ӧ�ӿ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������Һ�����ʵ����ʵ���Ũ��Ϊ1mol•L﹣1���ǣ�������
��-A��-��58.5 g NaCl�ܽ���1 Lˮ����ɵ���Һ
��-B��-��K+Ϊ2 mol��K2SO4��Һ
��-C��-��0.5 mol•L﹣1��NaNO3��Һ100 mL����������50 gˮ����Һ
��-D��-��250 g ��������ˮ�����1 L��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ��һ����ʵ��Ϊ��������Ȼ��ѧ����ѧʵ���ڻ�ѧѧϰ�о��м�����Ҫ�����ã�����ʵ������ѡ�õ�������������ǣ�������
����50mL��Ͳ��ȡ35.20 mLϡ���ᡡ
���÷�Һ©�����뱽�����Ȼ�̼�Ļ����
����������ƽ����11.7g�Ȼ��ƾ���
��100mL������ƿ��ȡ100mLϡ����
�����������ж���ʯ��ʯ
����250mL����ƿ����250mL 0.2mol•L﹣1��NaOH��Һ��
��-A��-�٢ڢ�-B��-�ۢ�-C��-�ۢܢ�-D��-�ۢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧʵ��Ҫע�ⰲȫ��������Ϊ���ϰ�ȫҪ����ǣ�������
| �� | A�� | �����Ż�ʱ��������ˮ��� |
| �� | B�� | ϡ��Ũ����ʱ����ˮ����Ũ������ |
| �� | C�� | ŨNaOH��Һ����Ƥ���ϣ�������ˮ��ϴ��Ȼ��Ϳ��ϡ������Һ |
| �� | D�� | Ũ���ὦ��Ƥ���ϣ�������ϡNaOH��Һϴ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и���������ԭ����Ŀ�����ɴ�С˳�����е��ǣ�������
��0.5mol NH3 �ڱ�״����22.4L���� ��4��9mLˮ ��0.2mol H3PO4��
| �� | A�� | �٢ܢۢ� | B�� | �ܢۢڢ� | C�� | �ڢۢܢ� | D�� | �٢ܢڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1��0.25molH3PO4�����к�����ԭ�ӵ����ʵ�����������������ԭ����ĿΪ����
��2��0.3molH2O��0.4molCO2�����ʵ���֮��Ϊ����������������Ŀ֮��Ϊ����������ԭ����Ŀ֮��Ϊ������
��3��19gij���۽����Ȼ��ACl2���к���0.4mol Cl﹣����ACl2��Ħ������������A�����ԭ��������������ACl2�Ļ�ѧʽ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��2mol SO2��2mol SO3���壬����̶�������ܱ���������һ�������·������з�Ӧ��2SO2+O2⇌2SO3��ƽ��ʱSO3Ϊn mol����ͬ�¶��£��ֱ������������ͬ������ܱ������м�����ʼ���ʣ�����ƽ��ʱSO3�����ʵ���һ������n mol���ǣ���
A�� 2mol SO2+1mol O2
B�� 4mol SO2+1mol O2
C�� 2mol SO2+1mol O2+2mol SO3
D�� 3mol SO2+1mol SO3
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com