
ij����ɫ����A�ڿ����е�ȼ������ʻ�ɫ�������ɵ���ɫ����B����A�ڿ�����¶�ã�����ɰ�ɫ����C����AͶ��ˮ������D�����壻E�ǵؿ��к������Ľ���Ԫ�صĵ��ʡ��ش��������⣺
��1��B�Ļ�ѧʽ��________��C��������_________��д��E��D��Һ��Ӧ�Ļ�ѧ����ʽ______��
��2����1molA��1molE�Ļ����Ͷ������ˮ�У����������ڱ�״���µ����Ϊ_____________��
��3��������������Ͷ�뵽���������ͭ�Ļ����Һ�У���ַ�Ӧ��ʣ�������ĩ��������ԭ�������۵�������ȣ���ԭ��Һ��H+��SO42-�����ʵ���Ũ��֮����______��
 �������Ӧ���⼯ѵϵ�д�
�������Ӧ���⼯ѵϵ�д� �ۺ��Բ�ϵ�д�
�ۺ��Բ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ��һ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���й������ʵ���Ũ�ȱ�����ȷ����
A��0.3 mol��L��1 Na2SO4��Һ�к���Na����SO�����ʵ���Ϊ0.9 mol
B��50mL 1 mol��L��1��KCl��Һ��100mL 0.5 mol��L��1MgCl2��Һ�У�Cl�������ʵ���Ũ�����
C����1 Lˮ����22.4 L�������ð�ˮ��Ũ����1 mol��L��1
D��10 ��ʱ0.35 mol��L��1��KCl������Һ100 mL��������5 gˮ������ȴ��10 ��ʱ���������ʵ���Ũ����Ϊ0.35 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ����������һ�и߶��ϵ��Ĵ��¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��0.05molNaOH����ֱ��������100mLҺ���У���Һ�ĵ��������仯�������
A������ˮ B��0.5 mol•L-1����
C��0.5 mol•L-1 ���� D��0.5 mol•L-1 ��ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ����������һ�и�һ�ϵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���������ӷ�Ӧ����ʽ���Ӧ�Ļ�ѧ����ʽ��ȷ����
A��Cu2++2OH-=Cu(OH)2�� CuSO4+2NH3��H2O= Cu(OH)2��+(NH4)2SO4
B��Ba2++SO42-=BaSO4�� Ba(OH)2+H2SO4=BaSO4��+2H2O
C��Cu+2Ag+=Cu2++2Ag Cu+2AgCl=2Ag+CuCl2
D��Ag++Cl-=AgCl�� AgNO3+NaCl=AgCl��+NaNO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ����������һ�и�һ�ϵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ײ��ϡ�������ֱ��Ϊ1nm��100nm�IJ��ϡ�����̼�������е�һ�֣�ij�о���������̼���ȵķ�ɢ������ˮ�У��õ��������Ǣ�����Һ ���ǽ��� �۾��ж�������� �ܲ�������Ĥ �ݲ�������ֽ ��ֹ�����ֺ�ɫ����
������ȷ����
A���٢ܢ� B���ڢۢ� C���ڢۢ� D���٢ۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ��һ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ƽ���������������Ϸ��������ձ��������ձ��зֱ�ʢ�����������������Һ����ƽ����ƽ��״̬�����ֱ������ձ��м����������������ͼ�������ģ���ַ�Ӧ�� ��
A����ƽ����ƽ���� B������ҵ�
C������Ҹ� D����ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ��һ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʵķ���������ǣ� ��
A������ʣ�CO2��Ca(OH)2��H2O��HNO3
B���NaOH��Ba(OH)2��Na2CO3��NH3•H2O
C�����������CaO��Na2O��FeO��Mn2O7
D����NH4NO3��KAl(SO4)2��NH4Cl��NaHCO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������ʡ�߶��������ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
�״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ���������ַ�Ӧԭ����
��CH3OH��g��+H2O��g���TCO2��g��+3H2��g������H=+49.0kJ•mol-1
��CH3OH��g��+1/2O2��g���TCO2��g��+2H2��g������H=-192.9kJ•mol-1
����˵����ȷ����
A��CH3OH��ȼ����Ϊ192.9kJ•mol-1
B����Ӧ���е������仯��ͼ��ʾ
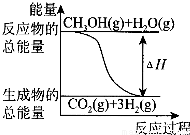
C��CH3OHת���H2�Ĺ���һ��Ҫ��������
D�����ݢ���֪��Ӧ��CH3OH��l��+1/2 O2��g��=CO2��g��+2H2��g���ġ�H��-192.9kJ•mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ�߶��ϵ��Ĵ��¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪�ױ���һ�ȴ�����4�֣���ױ���������ȫ�ӳɺ�IJ����һ�ȴ���Ӧ�þ��е���������
A��2�� B��4�� C��5�� D��7��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com