

| A. | 缬氨霉素是一种蛋白质 | |
| B. | 缬氨霉素完全水解可得到四种氨基酸 | |
| C. | 缬氨霉素完全水解后的产物中有两种产物互为同系物 | |
| D. | 缬氨霉素完全水解,其中一种产物与甘油互为同分异构体 |
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2L | |
| B. | 常温常压下,11.2LO2所含的原子数为NA | |
| C. | 0.5mol纯硫酸所含有的氧原子数与NA个CO2分子中所含有的氧原子数相等 | |
| D. | 标准状况下,11.2LCCl4含有的分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水久置变成稀盐酸 | |
| B. | 实验室用排饱和食盐水法收集氯气 | |
| C. | 合成氨反应加入催化剂以提高反应速率 | |
| D. | 由NO2、N2O4组成的混合气体,平衡后加压颜色先变深再变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
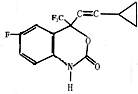 F是一种治疗艾滋病的新药(结构简式如图),已知F分子中苯环与-NH-CO-O-基团在同一平面内,关于F的以下说法正确的是( )
F是一种治疗艾滋病的新药(结构简式如图),已知F分子中苯环与-NH-CO-O-基团在同一平面内,关于F的以下说法正确的是( )| A. | F分子内最多可有13个碳原子在同一个平面内 | |
| B. | F分子内至少有8个碳原子在同一平面内 | |
| C. | F的水解产物一定都是极性分子 | |
| D. | 1molF与H2发生加成反应,消耗H2的物质的量最多是6mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
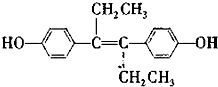 )是一种激素类药物,下列说法不正确的是( )
)是一种激素类药物,下列说法不正确的是( )| A. | 已烯雌酚分子中一定有16个碳原子共平面 | |
| B. | 已烯雌酚的分子式为C18H20O2,它为芳香族化合物 | |
| C. | 1 mol已烯雌酚可以与5 mol Br2发生反应 | |
| D. | 已烯雌酚能发生加成、取代、氧化、加聚、酯化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
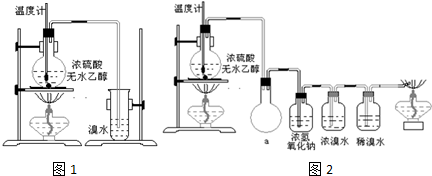
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.6 g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA | |
| B. | 氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2NA | |
| C. | 标准状况下,11.2 L苯中含有分子的数目为0.5NA | |
| D. | 在过氧化钠与水的反应中,每生成0.1 mol氧气,转移电子的数目为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com