
与6 g尿素[CO(NH2)2]含氮物质的量不相同的物质是
A.3.4 g NH3 B.0.1 mol NH4NO3
C.6 g NH4NO3 D.13.2 g(NH4)2SO4
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:

| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
| n(NH3) |
| n(CO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
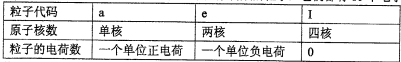
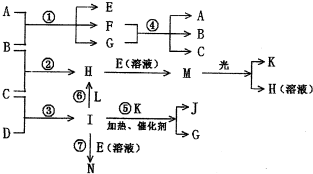


| ||
| ||


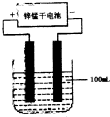
查看答案和解析>>
科目:高中化学 来源:重难点手册 高中化学·必修1 配人教版新课标 人教版新课标 题型:013
|
与6 g尿素[CO(NH2)2]含氮物质的量不相同的物质是 | |
| [ ] | |
A. |
3.4 g NH3 |
B. |
0.1 mol NH4NO3 |
C. |
6 g NH4NO3 |
D. |
13.2 g (NH4)2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com