
25��ʱ��0.1 mol Na2CO3�����������õ�һ�����Ϊ1 L����Һ����Һ�в�������pH �Ĺ�ϵ��ͼ��ʾ�������й���Һ������Ũ�ȹ�ϵ������ȷ����
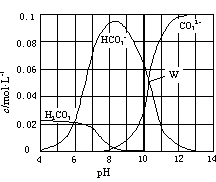 A��W����ʾ����Һ�У�
A��W����ʾ����Һ�У�
c(CO32��)��c(HCO3��)>c(OH��)> c(H+)
B��pH��4����Һ�У�
c(H2CO3)+ c(HCO3��)+ c(CO32��)��0.1 mol��L��1
C��pH��8����Һ�У�
c(Na+)>c(HCO3��) >c(H2CO3)>c(CO32��)
D��pH��11����Һ�У�
c(Na+)+ c (H+)��c(OH��)+c(Cl��)+ c(CO32��)+c(HCO3��)
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
1gN2��a�����ӣ����ӵ������ɱ�ʾΪ
A��a/28mol-1 B��a mol-1 C��28a mol-1 D��a/14 mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NA��ʾ�����ӵ���������ֵ��������������ȷ���ǣ� ��
A��1 mol NH3�����е�ԭ����ΪNA
B�����³�ѹ�£�22.4L����������ԭ����Ϊ2NA
C�����³�ѹ�£�48gO2��O3�Ļ������������ԭ����Ϊ3NA
D��1 L 0.1 mol/LNaCl��Һ��������Na+ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����£����и���������ָ����Һ��һ���ܴ����������
A�������̪����ɫ����Һ�У�K����Al3����Cl����CO32-
B���������Һ�У�Na����K����MnO4����AlO2��
C��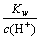 ��10-13 mol��L��1����Һ��Na����[Ag(NH3)2]����OH����NO3��
��10-13 mol��L��1����Һ��Na����[Ag(NH3)2]����OH����NO3��
D��c(I��)��0.1 mol��L��1����Һ�У�Na����H����ClO����SO42-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ͼʾ���Ӧ�������������
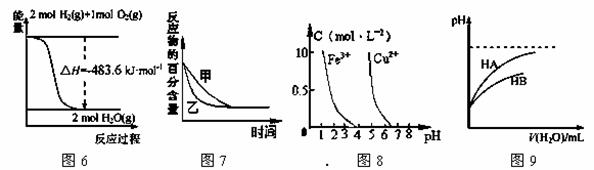 A��ͼ6��ʾH2��O2������Ӧ�����е������仯����H2��ȼ����Ϊ241.8 kJ��mol��1
A��ͼ6��ʾH2��O2������Ӧ�����е������仯����H2��ȼ����Ϊ241.8 kJ��mol��1
B��ͼ7��ʾѹǿ�Կ��淴Ӧ2A(g)+2 B(g) 3C(g)+D��s����Ӱ�죬�ҵ�ѹǿ�ȼ�ѹǿ��
3C(g)+D��s����Ӱ�죬�ҵ�ѹǿ�ȼ�ѹǿ��
C������ͼ8������ȥCuSO4��Һ�е�Fe3+��������Һ�м�������CuO������pH��4������
D��ͼ9��ʾ�����£�ϡ��HA��HB�������ϡ��Һʱ����ҺpH���ˮ���ı仯������ͬ������NaA��Һ��pH����ͬŨ�ȵ�NaB��Һ��pH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
þ�Ǻ�ˮ�к����϶�Ľ�����þ�Ͻ���þ�Ļ�������;�dz��㷺��
��1��Mg2Ni��һ�ִ���Ͻ���֪��
Mg(s) + H2(g) �� MgH2(s) ��H1����74.5kJ��mol��1
Mg2Ni(s) + 2H2(g) �� Mg2NiH4(s) ��H2����64.4kJ��mol��1
Mg2Ni(s)+2MgH2(s) �� 2Mg(s)+Mg2NiH4(s) �ġ�H3�� �� ��
��2��һ����ˮ��þʯ(��Ҫ�ɷ�ΪMgCl2��6H2O)�Ʊ�����þ���յĹؼ��������£�
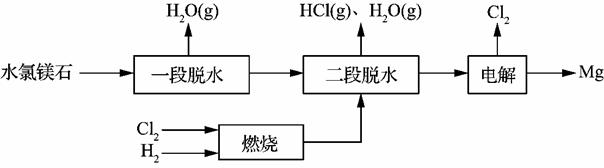
��Ϊ̽��MgCl2•6H2O��һ����ˮ���ĺ����¶ȷ�Χ��ij����С�齫MgCl2•6H2O�ڲ�ͬ�¶��·ֽ⣬��ò����������ʵ�X-����������ͼ����ͼ��ʾ��X-��������������ж�ij��̬�����Ƿ���ڣ���
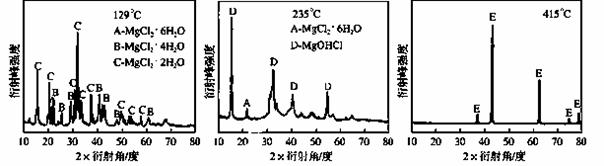
���E��MgԪ����������Ϊ60.0%����E�Ļ�ѧʽΪ �� ��
��һ����ˮ����Ŀ�����Ʊ�MgCl2��2H2O���¶Ȳ�����180 ���ԭ���� �� ��
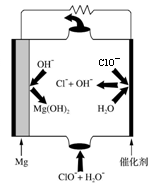 �������ʱ��������ˮ�֣������ɵ�MgOHCl������������Mg��Ӧ��ʹ�����������MgO�ۻ�Ĥ�����͵��Ч�ʡ�����MgO�Ļ�ѧ����ʽΪ �� ��
�������ʱ��������ˮ�֣������ɵ�MgOHCl������������Mg��Ӧ��ʹ�����������MgO�ۻ�Ĥ�����͵��Ч�ʡ�����MgO�Ļ�ѧ����ʽΪ �� ��
�۸ù����У�����ѭ��ʹ�õ������� �� ��
��3���������Mg(AlH4)2��110-200��C�ķ�ӦΪ��
Mg(AlH4)2��MgH2 +2A1+3H2��
ÿ����27gAlת�Ƶ��ӵ����ʵ���Ϊ �� ��
��4����þ-�������Ρ�ȼ�ϵ�ص�װ������ͼ��ʾ���õ�ص�������ӦʽΪ �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
X��Y��Z�����ڱ������ڵ����ֶ�����Ԫ�أ�X��Yͬ���ڣ�Y��Zͬ���壬����Ԫ��ԭ�ӵ�����������֮��Ϊ17��������֮��Ϊ31����X��Y��Z�ֱ���(����)
A��Mg��Al��Si B��Li��Be��Mg
C��N��O��S D��P��S��O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
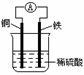
��ͼΪͭ��ԭ���ʾ��ͼ�������й�˵����ȷ���ǣ� ��
A��ͭ�����ܽ� B����װ���ܽ�����ת��Ϊ��ѧ��
C������������ͨ����������ͭ�� D��������ӦΪFe��2e����Fe2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ȡһ�������ľ��ȹ�������Cu��Cu2O�� CuO������ֳ����ȷݣ�ȡ����һ����������������ԭ����÷�Ӧ�������������6.40g����һ���м���500mLϡ���ᣬ����ǡ����ȫ�ܽ⣬��ͬʱ�ռ�����״����NO����4.48L����������������ʵ���Ũ��Ϊ
A��2.8mol��L B��3.2mol��L
B��3.2mol��L C��3.6mol��L
C��3.6mol��L D�����ж�
D�����ж�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com