
下列离子方程式正确的是
A.用铜作电极电解饱和食盐水:2Cl-+2H2O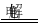 2OH-+Cl2↑+H2↑
2OH-+Cl2↑+H2↑
B.Fe3O4与过量的稀HNO3反应 : Fe3O4+8H+
: Fe3O4+8H+  Fe2++2Fe3++4H2O
Fe2++2Fe3++4H2O
C.向Ba(OH)2 溶液中逐滴加入NaHSO4溶液至Ba2+刚好沉淀完全:
Ba2++OH-+H++SO42-=BaSO4↓+H2O
D.NaHS溶液呈碱性:HS-+H2O H3O++OH-+S2-
H3O++OH-+S2-
科目:高中化学 来源:2017届云南省高三上第三次月考化学卷(解析版) 题型:选择题
物质中杂质(括号内为杂质)的检验、除杂的试剂或方法都正确的是( )
选项 | 物质及其杂质 | 检验方法 | 除杂 |
A | Cl2(HCl) | 通入AgNO3溶液中 | 饱和食盐水 |
B | FeCl2溶液(FeCl3) | 滴入KSCN溶液 | 通入过量氯气 |
C | 苯(苯酚) | 滴入FeCl3溶液 | 碱洗分液 |
D | KNO3晶体(NaCl) | 焰色反应 | 重结晶 |
查看答案和解析>>
科目:高中化学 来源:2017届山西省高三上10月阶段测化学卷(解析版) 题型:填空题
已知铁的化合物之间有如下转化关系,

请回答下列有关问题:
(1)Fe与过量稀盐酸反应可以制取FeCl2。若用反应所得的酸性溶液,实现上述①的转化,要求产物纯净,可选用的试剂是_________(选填序号);
a.KMnO4 b.HNO3 c.H2O2
(2)硫酸铁可用于电化浸出黄铜矿精矿工艺。精矿在阳极浸出的反应比较复杂,其中 有一主要反应:CuFeS2+4Fe3+=Cu2++5Fe2++2S。(CuFeS2中S为-2价)则下列说法正确的是_________(选填序号);
有一主要反应:CuFeS2+4Fe3+=Cu2++5Fe2++2S。(CuFeS2中S为-2价)则下列说法正确的是_________(选填序号);
a.从物质分类的角度看,黄铜矿属于合金
b.Cu2+和S是氧化产物
c.当转移1mol电子时,46g CuFeS2参加反应
d.反应中,CuFeS2既作氧化剂又作还原剂
(3)在FeCl3、CuCl2混合溶液中,加入一定量的铁屑,反应完全后将固体滤出。
①若滤出的固体中只有铜,则溶液中一定含有的阳离子是 ,一定不含的阳离子是 。
②若滤出的固体中含有铁和铜,则溶液中一定不含的阳离子是 。
(4)高酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,和水发生水解反应生成Fe(OH)3胶体等物质,写出FeO42- 和H2O反应的离子方程式 。高酸钾作为水处理剂发挥的作用是_____________、_____________。 (用简洁的名词描述即可)
查看答案和解析>>
科目:高中化学 来源:2017届山西省高三上10月阶段测化学卷(解析版) 题型:选择题
根据下表信息,下列叙述中正确的是
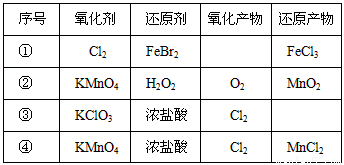
A.表中①反应的氧化产物只能有FeCl3
B.表中②生成1mol的O2将有4mol的电子转移
C.还原性比较:H2O2>Mn2+>Cl-
D.表中④的离子方程式配平后,H+的化学计量数为16
查看答案和解析>>
科目:高中化学 来源:2017届山西省高三上10月阶段测化学卷(解析版) 题型:选择题
下列现象或事实可用同一原理解释的是
A.浓硫酸和浓盐酸长期暴露在空气中浓度降低 B.次氯酸和双氧水使品红试液褪色
C.氯水和水玻璃长期暴露在空气中变质 D.苯和乙烯使溴水褪色
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江大庆一中高三上第二次月考化学试卷(解析版) 题型:选择题
下列有关溶液中离子的转化的表达合理的是( )
A.向0.1mol/L、pH=1的NaHA溶液中加入NaOH溶液:HA-+OH-=A2-+H2O
B.用CH3COOH溶解CaCO3: CaCO3+2H+= Ca2++H2O+CO2↑
C.含有0.2molFeI2的溶液中加入0.25 molBr2: 2Fe2++4I-+3Br2=2Fe3++2I2+6Br-
D.向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液使SO42-完全沉淀:
NH4++Al3++2SO42-+2Ba2++4OH-=NH3·H2O+Al(OH)3↓+2BaSO4↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com