
一定条件下,可逆反应C(s)+CO2(g)  2CO(g) ΔH>0,达到平衡状态,现进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积;④减小体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的是 ( )
2CO(g) ΔH>0,达到平衡状态,现进行如下操作:①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积;④减小体系中CO的量。上述措施中一定能使反应的正反应速率显著加快的是 ( )
| A.①②③④ | B.①③ | C.①② | D.①③④ |
B
解析试题分析:影响化学反应速率的因素有浓度、温度、压强、催化剂等。①升高温度,化学反应的正反应、逆反应的速率都加快。②由于碳单质是固体,所以增加反应物C的用量,化学反应速率不变。③缩小反应体系的体积。反应物、生成物的浓度都增大,反应速率加快。④减小体系中CO的量即减小生成物的浓度。在这一瞬间,由于反应物的浓度不变,正反应速率不变。生成物的浓度减小,V正>V逆,化学平衡正向移动。随着反应的进行,反应物的浓度逐渐减小 ,正反应速率逐渐减慢,最终正反应、逆反应速率相等,达到新的平衡状态。故上述措施中一定能使反应的正反应速率显著加快的是 ①③。选项为:B。
考点:考查外界条件对化学反应速率的影响。


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:单选题
认真研读课本是一种良好的学习习惯、按照课本所述,下列说法不正确的是( )
| A.护发素的主要功能是调节头发的pH,使之达到适宜的酸碱度 |
| B.厕所清洁剂、醋、肥皂、厨房清洁剂的pH依次增大 |
| C.仅用1mol/L KI溶液、0.1mol/L H2SO4溶液和淀粉溶液(仪器不限),就可以探究温度对化学反应速率的影响 |
| D.将少量Mg(OH)2沉淀和适量氯化铵溶液混合,无明显现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在一定温度下,在固定容积的密闭容器中,可逆反应H2(g)+ Br2(g)  2HBr(g)达到平衡的标志是
2HBr(g)达到平衡的标志是
| A.断裂1 mol H-H键的同时生成2 mol H-Br键 |
| B.单位时间内消耗1 mol H2,同时生成1 mol Br2 |
| C.H2、Br2、HBr的分子数之比为1∶1∶2 |
| D.混合气体的压强不再改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在密闭容器中发生下列反应aA(g) cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,C的浓度为原平衡的1.6倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,C的浓度为原平衡的1.6倍,下列叙述正确的是
| A.A的转化率变大 | B.平衡向正反应方向移动 |
| C.D的质量分数变大 | D.a<c+d |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在密闭容器中进行如下反应:X2(g)+Y2(g)  2Z(g),在温度T1和T2时,产物的量与反应时间的关系如图所示.符合图示的正确判断是
2Z(g),在温度T1和T2时,产物的量与反应时间的关系如图所示.符合图示的正确判断是
| A.T1<T2,正反应是放热反应 | B.T1<T2,正反应是吸热反应 |
| C.T1>T2,正反应是放热反应 | D.T1>T2,正反应是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对于A2+3B2 2C的反应来说,以下化学反应速率的表示中,反应速率最快的是
2C的反应来说,以下化学反应速率的表示中,反应速率最快的是
A.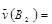 0.8mol·L-1·s-1 0.8mol·L-1·s-1 | B. 0.7mol·L-1·s-1 0.7mol·L-1·s-1 |
C. 0.4mol·L-1·s-1 0.4mol·L-1·s-1 | D.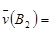 54mol·L-1·min-1 54mol·L-1·min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
硫代硫酸钠与稀盐酸的反应Na2S2O3+2HCl→2NaCl+S↓+SO2↑+H2O在加热条件下反应速度加快,原因主要是
| A.该反应是吸热反应,且可逆,加热使平衡向正向移动 |
| B.加热促使SO2逸出,使平衡向正向移动 |
| C.加热促进S2O32-与H+的碰撞,使反应加速 |
| D.加热促进Na+与Cl-的碰撞,使反应加速 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
反应A(g)+3B(g) 2C(g)+2D(g),在不同情况下测得反应速率,其中反应速率最快的是
2C(g)+2D(g),在不同情况下测得反应速率,其中反应速率最快的是
A.υ(D)=0.4 mol / (L·s) B.υ(C)=0.5 mol / (L·s)
C.υ(B)=0.6 mol / (L·s) D.υ(A)=0.15 mol / (L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对于可逆反应2HI(g)  I2(g)+H2(g),下列叙述能够说明已达到平衡状态的是
I2(g)+H2(g),下列叙述能够说明已达到平衡状态的是
| A.各物质的量的浓度比2 : 1: 1 |
| B.容器内的总压不随时间变化 |
| C.生成2 mol H-I键的同时生成1 mol I-I键 |
| D.混合气体的颜色不再变化时 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com