
| A.硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑ |
| B.NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O |
| C.小苏打溶液中加足量Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3↓+2H2O+CO32- |
| D.将足量的铁丝投入稀硝酸中:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O |
 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源:不详 题型:填空题
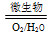 Fe2++SO42—
Fe2++SO42—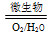 Fe3+这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为_____________________________,
Fe3+这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为_____________________________,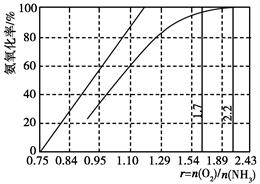
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 实验步骤 | 实验现象 |
| 将打磨过的铝片(过量)放入一定浓度的CuCl2溶液中 | 产生气泡,析出疏松的红色固体,溶液逐渐变为无色 |
| 反应结束后分离出溶液备用 | |
| 红色固体用蒸馏水洗涤后,置于潮湿空气中 | 一段时间后固体由红色变为绿色[设其主要成分为Cu2(OH)2CO3] |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.新制的氧化铝溶于氢氧化钠溶液:Al2O3+2OH- 2Al 2Al +H2O +H2O |
B.冷的氢氧化钠溶液中通入氯气:Cl2+OH- Cl-+HClO Cl-+HClO |
C.用KIO3氧化酸性溶液中的KI:5I-+I +3H2O +3H2O 3I2+6OH- 3I2+6OH- |
D.硫酸铝溶液中加入过量氨水:Al3++3OH- Al(OH)3↓ Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
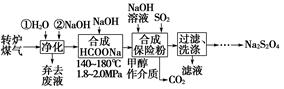
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
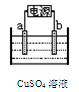

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将铜屑加入Fe3+溶液中:2Fe3++Cu=2Fe2++Cu2+ |
| B.将磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O |
C.将氯化亚铁溶液和稀硝酸混合:Fe2++4H++ =Fe3++2H2O+NO↑ =Fe3++2H2O+NO↑ |
| D.将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.用惰性电极电解饱和食盐水:2Cl-+2H2O Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
B.苯酚与碳酸钠溶液: + CO32—→ + CO32—→ + H2CO3 + H2CO3 |
| C.等体积等物质的量浓度的NH4Fe(SO4)2和Ba(OH)2混合:2Fe3++ 3SO42-+ 3Ba2++6OH-→3BaSO4↓+ 2Fe(OH)3↓ |
| D.在强碱性溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3→2FeO42-+3Cl-+ H2O+4H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com