
| A、原子组成一样 |
| B、O-H键的化学键类型一样 |
| C、羟基中氢原子活性性不同 |
| D、酚羟基能发生电离,醇羟基也能发生电离 |


 提分百分百检测卷系列答案
提分百分百检测卷系列答案科目:高中化学 来源: 题型:
 且a、b、c、d均大于零,则下列说法正确的是( )
且a、b、c、d均大于零,则下列说法正确的是( )| A、断开1molH-Cl键所需的能量为-a-b-c |
| B、b>c,则氢气分子具有的能量高于氯气分子具有的能量 |
| C、Cl2(s)=Cl2(g)△H=+(a+d)kJ?mol-1 |
| D、向1molCl2(g)中通入1molH2(g),发生反应时放热dkJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝制器皿不宜盛放酸性食物 |
| B、电解食盐水时阴极产生氢气 |
| C、可用铁制容器盛放和运输浓硫酸 |
| D、镀锌铁桶镀层破损后铁仍不易被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 充电 |
| 放电 |
| A、构成该电池的正极和负极必须是两种活性不同的金属 |
| B、充电时有CH3OH生成的电极为阳极 |
| C、放电时负极的电极反应为:CH3OH-6e-+8OH-=CO32-+6H2O |
| D、充电时每生成1 mol CH3OH转移12mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分液、蒸发、萃取 |
| B、分液、萃取、加热 |
| C、分液、蒸馏、萃取 |
| D、蒸馏、加热、蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
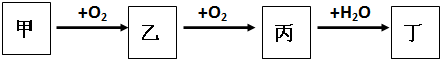
查看答案和解析>>
科目:高中化学 来源: 题型:
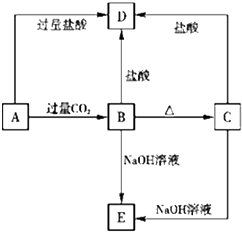 A、B、C、D、E五种化合物,均含有前18号元素中某种常见元素,它们的转化关系如图所示,其中A为澄清溶液,C为难溶的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃).
A、B、C、D、E五种化合物,均含有前18号元素中某种常见元素,它们的转化关系如图所示,其中A为澄清溶液,C为难溶的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃).查看答案和解析>>
科目:高中化学 来源: 题型:
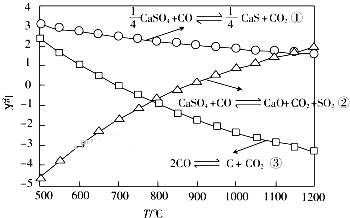 一氧化碳在高温下可还原硫酸钙,相关反应的平衡常数的对数与反应温度的关系如图所示.
一氧化碳在高温下可还原硫酸钙,相关反应的平衡常数的对数与反应温度的关系如图所示.| 1 |
| 4 |
| 1 |
| 4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com