
【题目】以粉煤灰(主要含Al2O3、SiO2,还有少量的Fe2O3)为原料制取Al2O3的流程如下:
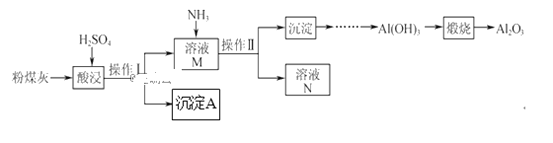
(1)操作Ⅰ的名称是__。
(2)用H2SO4“酸浸”时的离子方程式为__(任写一个)。
(3)简述如何检验酸浸后溶液中是否有Fe3+__。
(4)“煅烧”时的化学方程式为__。
(5)沉淀A与氢氟酸反应的化学方程式为__。
【答案】过滤 Fe2O3+6H+=2Fe3++3H2O(或Al2O3+6H+=Al3++3H2O任写一个) 取适量该溶液于试管中,加入KSCN,若变红则有Fe3+ 2Al(OH)3![]() Al2O3+3H2O SiO2+4HF=SiF4↑+2H2O
Al2O3+3H2O SiO2+4HF=SiF4↑+2H2O
【解析】
粉煤灰(主要含Al2O3、SiO2, 还有少量的Fe2O3)和稀硫酸混合,发生反应Al2O3+3H2SO4═Al2(SO4)3+3H2O,Fe2O3+3H2SO4═Fe 2(SO4)3+3H2O,SiO2和稀硫酸不反应,过滤溶液得滤渣Ⅰ为SiO2; 根据Fe3+遇KSCN溶液变红色检验溶液中是否有Fe3+;Al(OH)3加热分解为Al2O3和水;SiO2与氢氟酸反应生成SiF4和水。
(1)操作Ⅰ实现了固体SiO2和溶液的分离,操作Ⅰ的名称是过滤。
(2)用H2SO4“酸浸”时Al2O3、Fe2O3与硫酸反应,反应的离子方程式分别为Al2O3+6H+=Al3++3H2O、Fe2O3+6H+=2Fe3++3H2O。
(3)Fe3+遇KSCN溶液变红色,检验溶液中是否有Fe3+的方法是:取适量该溶液于试管中,加入KSCN,若变红则有Fe3+。
(4)“煅烧”时Al(OH)3分解为Al2O3和水,化学方程式为2Al(OH)3![]() Al2O3+3H2O。
Al2O3+3H2O。
(5)沉淀A是SiO2,SiO2与氢氟酸反应生成SiF4和水,化学方程式为SiO2+4HF=SiF4↑+2H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】自然界中时刻存在着氮的转化。实现氮按照一定方向转化一直是科学领域研究的重要课题,如图为N2分子在催化剂的作用下发生的一系列转化示意图:
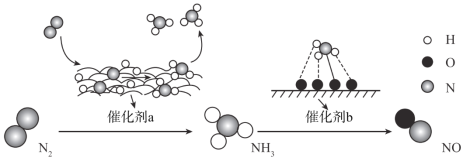
下列叙述正确的是
A.N2![]() NH3,NH3
NH3,NH3![]() NO均属于氮的固定
NO均属于氮的固定
B.催化剂a作用下氮原子发生了氧化反应
C.催化剂a、b表面均发生了极性共价键的断裂
D.使用催化剂a、b均可以提高单位时间内生成物的产量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(H2C2O4)是一种二元弱酸,在菠菜、苋菜、甜菜等植物中含量较高。25℃时,向H2C2O4溶液中滴加NaOH溶液,混合溶液中lgX [X表示 ![]() 或
或![]() 随pH的变化关系如图所示。下列说法不正确的是 ( )
随pH的变化关系如图所示。下列说法不正确的是 ( )
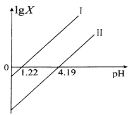
A.直线I中X表示的是![]()
B.直线I、Ⅱ的斜率均为1
C.0.1mol/ L NaHC2O4溶液中:c(Na+)>c(HC2O4-)> c(C2O42-)> c(H2C2O4)
D.已知:25℃时,NH3·H2O的电离常数为10-4.69,则(NH4)2C2O4溶液呈碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应A2(g) + B2(g)=2AB(g) 的能量变化如图所示,下列叙述中正确的是( )
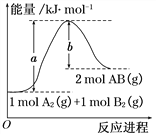
A.每生成2mol AB(g) 共吸收b kJ热量
B.该反应热ΔH = +(a-b) kJ·mol-1
C.反应物的总能量大于生成物的总能量
D.断裂1 mol A—A键,放出a kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同温度下,水溶液中-lg c(H+)与-lg c(OH)。关系如图所示。下列说法不正确的是( )
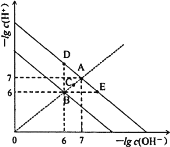
A.图中五点Kw间的关系:B>C>A=D=E
B.A→E点对应的水溶液中,可能有NH4+、Ba2+、Cl、I大量同时存在
C.若0.1mol·L1的NaHA溶液水溶液中c(H+)与c(OH)关系如图D点所示,则溶液中有:c(HA)>c(OH)>c(A2)>c(H2A)
D.向NaHSO4溶液中滴入Ba(OH)2溶液,当c(H+)与c(OH)关系如图E点所示,则溶液中反应:2H++SO42-+Ba2++2OH=BaSO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物。
某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究。
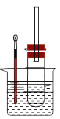
实验操作Ⅰ:在试管中加入5 mL 1 mol/L NaOH溶液和5 mL 溴乙烷,振荡。
实验操作II:将试管如图固定后,水浴加热。
(1)用水浴加热而不直接用酒精灯加热的原因是_______________________________。
(2)观察到_________________________现象时,表明溴乙烷与NaOH溶液已完全反应。
(3)鉴定生成物中乙醇的结构,可用的波谱是_________________________________。
(4)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的是______________________,检验的方法是_____________(需说明:所用的试剂、简单的实验操作及预测产生的实验现象)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组研究大小相同、过量的去膜镁条与40mL0.1mol·L1的盐酸和醋酸分别反应,相同条件下测得气体体积与反应时间关系如下表所示:
气体读数/mL | 5 mL | 10 mL | 15 mL | 20 mL | …… | 45 mL |
A瓶(醋酸)/s | 155 | 310 | 465 | 565 | …… | 865 |
B瓶(盐酸)/s | 7 | 16 | 30 | 64 | …… | 464 |
下列说法不正确的是( )
A.0~5mL时,A与B反应速率不同的原因是c(H+)不同所致
B.5~10mL时,A瓶平均反应速率为![]() mL·s1
mL·s1
C.0~20mL时,A瓶反应速率增大,可能是温度升高所致
D.0~45mL时段内,镁与盐酸反应的速率始终大于镁与醋酸反应的速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2(g)+O2(g)═2H2O(g)△H1
3H2(g)+Fe2O3(s)═2Fe(s)+3H2O(g)△H2
2Fe(s)+![]() O2(g)═Fe2O3(s)△H3
O2(g)═Fe2O3(s)△H3
2Al(s)+![]() O2(g)═Al2O3(s)△H4
O2(g)═Al2O3(s)△H4
2Al(s)+Fe2O3(s)═Al2O3(s)+2Fe(s)△H5
下列关于上述反应焓变的判断正确的是( )
A.△H1<0,△H3>0B.△H5<0,△H4<△H3
C.△H1=△H2+△H3D.△H3=△H4+△H5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据事实,写出下列反应的热化学方程式。
(1)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为___。
(2)已知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com