
【题目】下列物质中,含有非极性共价键的是( )
A.CaCl2
B.CO2
C.Na2O2
D.CH4
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:2H2(g)+O2(g)===2H2O(g)ΔH1=-483.6kJ/mol
则对于热化学方程式:2H2O(l)===2H2(g)+O2(g)ΔH2=QkJ/mol
下列说法正确的是
A.热化学方程式中化学计量数表示分子个数 B.Q = 483.6
C.Q > 483.6 D.Q < 483.6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据最新报道:用10B合成的10B20分子由非常好的抗癌作用,下列说法正确的是( )
A.10B的质子数是10
B.10B20是一种新合成的化合物
C.10B的中子数与核外电子数相同
D.B元素位于元素周期表中的第三列
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法错误的是( )
A. 若1 mol·L-1 HF溶液中H+数目为NA,则等体积的2 mol·L-1 HF溶液中H+数目为2NA
B. 44 g CO2、N2O组成的混合气体中所含有的原子数为3NA
C. 36 g 3H2中含有的中子数目为24NA
D. 2.24 L O2与钠反应时,转移电子数目可能为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)向某 NaOH 溶液中投入一块 Al箔,先无明显现象,随后逐渐产生气泡,则产生气泡的离子反应方程式为_________________________。
(2)实验室常用还原性 Fe 粉与水蒸气反应的实验来研究 Fe 的还原性,则该反应的化学反应方程式为_________________________。
(3)Fe(OH)2 制备时,采用的方法是“长滴管、液面下”的实验操作,但在实验时,由于操作不当,依旧会出现白色沉淀、灰绿色沉淀直至最终变为红褐色沉淀,写出白色沉淀最终转化为红褐色沉淀的化学反应方程式为________________________。
(4)实验时制备 Al(OH)3 时,常用可溶性铝盐(如 Al2(SO)4)与氨水反应进行制备。某课外小组在实验时不慎向 Al2(SO)4 溶液中加入了过量 NaOH 溶液,最终并没有制出白色沉淀 Al(OH)3,则该小组同学实验时发生的总离子反应方程式为______________________。
(5)充分煅烧 CoC2O4 后可得到 2.41g 钴的氧化物和 1.344L(标准状况)CO2 气体,则生成钴的氧化物的化学式为________________,煅烧 CoC2O4 的化学反应方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨是人类科学技术上的一项重大突破,其反应原理为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ·mol-1。一种工业合成氨的简式流程图如下:
2NH3(g) ΔH=-92.4 kJ·mol-1。一种工业合成氨的简式流程图如下:
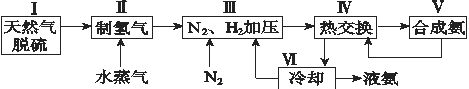
(1)天然气中的H2S杂质常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式:_______________。
(2)步骤Ⅱ中制氢气的原理如下:
①CH4(g)+H2O(g)![]() CO(g)+3H2(g) ΔH=+206.4 kJ·mol-1
CO(g)+3H2(g) ΔH=+206.4 kJ·mol-1
②CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
对于反应①,一定可以提高平衡体系中H2的百分含量,又能加快反应速率的措施是 __。
利用反应②,将CO进一步转化,可提高H2的产量。若1 mol CO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18 mol CO、CO2和H2的混合气体,则CO的转化率为____________。
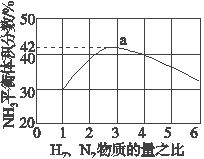
(3)如图表示500 ℃、60.0 MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数:______________。
(4)上述流程图中,使合成氨放出的能量得到充分利用的主要步骤是(填序号)_____________。简述本流程中提高合成氨原料总转化率的方法:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中A~J均为中学化学中常见的物质,它们之间有如下转化关系。其中A、D 为生活中常见金属单质。(反应过程中生成的水及其他产物已略去)
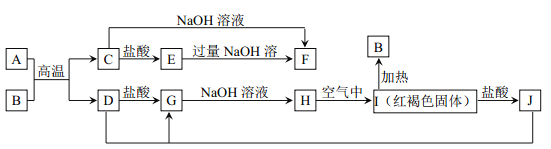
请回答以下问题:
(1)A 是_________,B是_________。(填化学式)
(2)A与B高温反应制得金属 D 的化学反应方程式为________________________。
(3)J的溶液可用来 “刻蚀”铜质电路板,在该刻蚀过程中,所发生反应的离子方程式为_________________________。
(4)检验J中阳离子的试剂是______________________。(写试剂名称)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能源是一种重要的清洁能源。现有两种可产生H2的化合物甲和乙。将 6.00 g 甲加热至完全分解,只得到一种常见金属单质和 6.72 L 的 H2(已折算成标准状况)。甲与水反应也能放出H2,同时还产生一种白色沉淀物,该白色沉淀既可以溶于盐酸,也可溶于 NaOH 溶液。化合物乙在催化剂存在下可分解得到H2 和另一种单质气体丙,丙在标准状况下的密度为1.25 g·L-1。请回答下列问题:
(1)甲是_______________;乙是______________。( 填化学式)
(2)甲与水反应的化学方程式是____________。
(3)气体丙的分子式是____________。
(4)乙在加热条件下可与 CuO 发生反应,生成红色固体和气体丙,写出该反应的化学方程式________________。
(5)有人提出产物Cu中可能还混有Cu2O,请设计实验方案验证:__________________。
(已知:Cu2O+2H+=Cu+Cu2++H2O;Cu、Cu2O 均可以溶解在 HNO3 溶液中)
(6)甲与乙之间_____________ (填“可能”或“不可能”)发生反应产生H2,判断理由是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各实验装置的叙述中,不正确的是
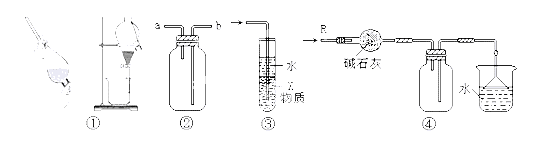
A.装置①可用于分离CH3CHO和H2O的混合物
B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体
C.装置③中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸
D.装置④可用于干燥、收集NH3,并吸收多余的NH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com