
| A.金刚石>晶体硅>二氧化硅>碳化硅 | B.CI4>CBr4>CCl4>CF4 |
| C.K2O>Na2O>O2>N2 | D.干冰 >二氧化硅>氯化钠>钠 |
科目:高中化学 来源:不详 题型:填空题
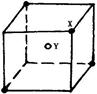
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
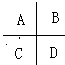
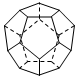
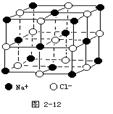
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
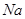 、
、 、
、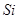 、
、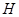 、
、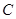 、
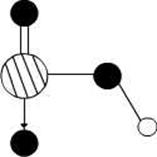
、 等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。 (1)图中d的单质对应元素原子的电子排布式是
等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。 (1)图中d的单质对应元素原子的电子排布式是  键, 个
键, 个 键。
键。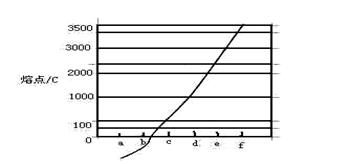
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.晶体在三维空间里呈周期性有序排列,因此在各个不同的方向上具有相同的物理性质 |
| B.晶体在熔化过程中需要不断的吸热,温度不断地升高 |
| C.普通玻璃在各个不同的方向上力学、热学、电学、光学性质相同 |
| D.晶体和非晶体之间不可以相互转化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaCl晶体中每个Na+周围同时吸引6个Cl- |
| B.干冰晶体中每个CO2分子周围与它距离最近且等距的CO2分子有12个 |
| C.金刚石晶体中最小的碳环为六元环,为平面正六边形 |
| D.石墨晶体中每个碳原子与其他3个碳原子间形成共价键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 线,计算出NaCl固体的体积为VmL。回答下列问题:
线,计算出NaCl固体的体积为VmL。回答下列问题: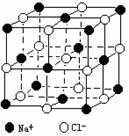
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com