
| A. | 等物质的量浓度等体积的稀硫酸和氢氧化钡溶液反应 | |
| B. | 稀硫酸和过量氢氧化钡溶液反应 | |
| C. | 硫酸氢钠溶液和过量氢氧化钡溶液反应 | |
| D. | 硫酸氢钠溶液和少量氢氧化钡溶液反应 |
分析 A.等物质的量浓度等体积的稀硫酸和氢氧化钡溶液反应生成硫酸钡和水;
B.稀硫酸和过量氢氧化钡溶液反应生成硫酸钡和水;
C.该离子方程式可以表示氢氧化钡与少量的硫酸氢钠的反应;
D.硫酸氢钠溶液和少量氢氧化钡溶液反应生成硫酸钡和水、硫酸钠.
解答 解:A.等物质的量浓度等体积的稀硫酸和氢氧化钡溶液反应,离子方程式:Ba2++SO42-+2H++2OH-=2H2O+BaSO4↓,故A错误;
B.稀硫酸和过量氢氧化钡溶液反应,离子方程式:Ba2++SO42-+2H++2OH-=2H2O+BaSO4↓,故B错误;
C.硫酸氢钠溶液和过量氢氧化钡溶液反应,反应生成硫酸钡、氢氧化钠和水,离子方程式:H++SO42-+OH-+Ba2+═BaSO4↓+H2O,故C正确;
D.硫酸氢钠溶液和少量氢氧化钡溶液反应,离子方程式:Ba2++SO42-+2H++2OH-=2H2O+BaSO4↓,故D错误;
故选:C.
点评 本题考查了离子方程式的书写,注意掌握离子方程式、化学方程式的书写原则是解题关键,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:多选题
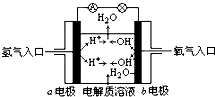
| A. | b电极是负极 | |
| B. | 总反应方程式为:2H2+O2═2H2O | |
| C. | 负极发生还原反应,正极发生氧化反应 | |
| D. | 氢氧燃料电池是一种具有广泛应用前景的绿色电源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2+F2═2HF | B. | 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$ 2Fe+3CO2 | ||
| C. | NaOH+HCl═NaCl+H2O | D. | 4HNO3$\frac{\underline{\;\;△\;\;}}{\;}$ 2H2O+4NO2↑+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 71 g Cl2所含原子数为2NA | |
| B. | 在常温常压下,1 mol氦气含有的原子数为2NA | |
| C. | 0.1L0.5mol/LCH3COOH溶液中含有的氢离子数为0.05NA | |
| D. | 标准状况下,1 mol H2O和1 mol H2的体积都约为22.4 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 32 g O2气体含有的氧原子数为NA | |
| B. | 2 L 0.3 mol/L Na2SO4溶液中含有Na+为0.6NA | |
| C. | 54 g铝完全反应后失去的电子数为6NA | |
| D. | 11.2 L氮气所含的分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 构成物质一定是化合物 | |
| B. | 构成物质一定是单质 | |
| C. | 构成物质可能只有一种元素 | |
| D. | 物质的组成元素一定是两种或两种以上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ•mol-1 | |
| B. | CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=+890kJ•mol-1 | |
| C. | CH4(g)+O2(g)═CO2(g)+H2O(l)△H=-890kJ•mol-1 | |
| D. | 2CH4(g)+4O2(g)═2CO2(g)+4H2O(g)△H=+890kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 往氨水中滴加酚酞 | B. | NO气体暴露在空气中 | ||
| C. | Cl2通过湿润的有色布条 | D. | 往NaOH溶液中通入CO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com