
“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是( )
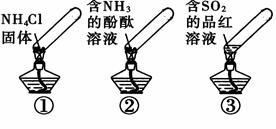
A. 加热时,①上部汇集了固体NH4Cl,说明NH4Cl的热稳定性比较好
B. 加热时,②溶液褪色或红色变浅,冷却后又都变为红色
C. 加热时,③溶液褪色或红色变浅,冷却后又都变为红色
D. 三个“封管实验”中所发生的化学反应都是可逆反应
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源:2016-2017学年四川省成都市高一入学考试化学卷(解析版) 题型:选择题
推理是化学学习中常用的思维方法,下列推理中正确的( )
A.酸中都含有氢元素,所以含有氢元素的化合物一定是酸
B.酸与碱反应有盐和水生成,因此有盐和水生成的反应一定是酸与碱反应
C.碱性溶液能使石蕊试液变蓝,所以能使石蕊试液变蓝的溶液一定呈碱性
D.碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
查看答案和解析>>
科目:高中化学 来源:2017届北京市央民族大学附高三上9.12周练化学卷(解析版) 题型:选择题
新型纳米材料氧缺位铁酸盐(MFe2Ox 3<x<4,M表示Mn、Co、Zn或Ni的二价离子),常温下,它能使工业废气中SO2、NO2等氧化物转化为单质。转化流程如图。有关上述转化过程的下列叙述正确的是
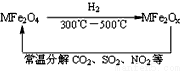
A.MFe2O4表现了还原性
B.MFe2Ox表现了还原性
C.SO2和NO2表现了还原性
D.SO2和NO2发生了分解反应
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古高三上第一次月考化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.0.1 mol·L-1 NaOH溶液:K+、Na+、SO42-、CO32-
B.0.1 mol·L-1 Na2CO3溶液:K+、Ba2+、NO3-、Cl-
C.0.1 mol·L-1 FeCl3溶液:K+、NH4+、I-、SCN-
D.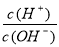 =1×1014的溶液:Ca2+、Na+、ClO-、NO3-
=1×1014的溶液:Ca2+、Na+、ClO-、NO3-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高二上起点考试化学卷(解析版) 题型:实验题
亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,使用过量会使人中毒,国际上对食品中亚硝酸钠的用量控制在很低的水平上。某学习小组针对亚硝酸钠设计了如下实验:
【实验I】制备NaNO2
该小组查阅资料知:2NO+Na2O2=2NaNO2; 2NO2+Na2O2=2NaNO3
设计制备装置如下(夹持装置略去):
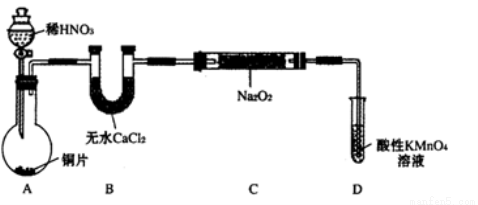
(1)装置D可将剩余的NO氧化成NO3-,发生反应的离子方程式为 。
(2)如果没有B装置,C中发生的副反应有 , 。
(3)甲同学检查完装置气密性良好后进行实验,发现制得的NaNO2中混有较多的NaNO3杂质。于是在A与B装置间增加了 装置, 改进后提高了NaNO2的纯度。
改进后提高了NaNO2的纯度。
【实验Ⅱ】测定制取的样品中NaNO2的含量
步骤:
a.在5个有编号的带刻度试管(比色管)中分别加入不同量的NaNO2溶液,各加入1 mL的M溶液(M遇NaNO2呈紫红色,NaNO2浓度越大颜色越深),再加蒸馏水至总体积均为10 mL并振荡,制成标准色阶:

b.称量0.10 g制得的样品溶于水配成500 mL溶液。取5 mL待测液,加入1 mL M溶液,后加蒸馏水至10 mL振荡,与标准色阶比较。
(4)步骤b中比较结果是:待测液颜色与③号色阶相同。则甲同学制得的样品中NaNO2的质量分数是 %。
(5)用目视比色法证明维生素C可以有效降低NaNO2的含量。设计并完成下列实验报告。
实验方案 | 实验现象 | 实验结论 |
取5mL待测液加入 ,振荡,再加入1ml M溶液 , ,再振荡,与③号色阶对比。 | 维生素C可以有效降低NaNO2 的含量。 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高二上起点考试化学卷(解析版) 题型:选择题
氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为:a HClO3 = bO2↑+ cCl2↑+ dHClO4 + eH2O用湿润的淀粉碘化钾试纸检验气体产物时,试纸先变蓝后褪色。下列说法正确的( )
A.由反应可确定:氧化性HClO4>HClO3
B.若化学计量数a=8,b=3,则该反应转移电子数为20e-
C.变蓝的淀粉碘化钾试纸褪色是因为可能发生了:4C12 + I2 + 6H2O = 12H+ + 8Cl-+ 2IO3-
D.若氯酸分解所得混合气体,lmol混合气体质量为47.6g,则反应方程式可表示为:26HClO3=15O2↑+ 8C12↑+ 10HClO4 + 8H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高二上起点考试化学卷(解析版) 题型:选择题
有下列六种转化途径,某些反应条件和产物已省略,下列有关说法正确的是( )
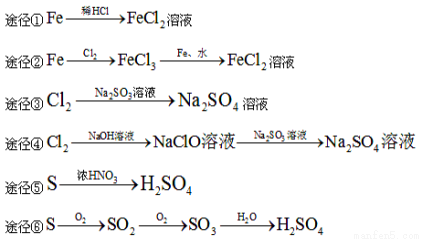
A.由途径①和②分别制取1molFeCl2,理论上各消耗1molFe,各转移2mole-
B.由途径③和④分别制取1 mol Na2SO4,理论上各消耗1 mol Cl2,各转移2mol e-
C.由途径⑤和⑥分别制取1 mol H2SO4,理论上各消耗1mol S,各转移6mol e-
D.以上说法都不正确
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三上9月月考理综化学试卷(解析版) 题型:实验题
氧化镁应用广泛。以菱镁矿(主要成分为MgCO3,SiO2和FeCO3)为原料制备高纯氧化镁的实验流程如下:

(1)MgCO3与稀硫酸反应的离子方程式为 。
(2)加入H2O2时,反应的离子方程式为 。
(3)滤渣1和滤渣2的成分分别是 (填化学式) 、 。
(4)煅烧过程存在以下反应:
2MgSO4+C 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑
MgSO4+3C MgO+S↑+3CO↑
MgO+S↑+3CO↑
①上述煅烧过程中产生的SO2用溴水吸收,离子方程式为__________________
②得到的淡黄色固体S与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上学期摸底考试化学试卷(解析版) 题型:填空题
锡及其化合物在生产、生活中有着重要的用途。已知:Sn的熔点为231℃;Sn2+易水解、易被氧化;SnCl4极易水解、熔点为-33 ℃、沸点为114 ℃。请按要求回答下列相关问题:
(1)元素锡比同主族碳的周期数大3,锡的原子序数为_______________。
(2)用于微电子器件生产的锡粉纯度测定:①取1.19 g试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;②加入过量的Fe2(SO4)3;③用0.1000 mol/L K2Cr2O7溶液滴定(产物中Cr呈+3价),消耗20.00 mL。步骤②中加入Fe2(SO4)3的作用是__________________;此锡粉样品中锡的质量分数_____________。
(3)用于镀锡工业的硫酸亚锡(SnSO4)的制备路线如下:

①步骤Ⅰ加入Sn粉的作用: __________________及调节溶液pH。
②步骤Ⅱ、步骤Ⅴ的操作名称为________________,写出该过程用到的一种玻璃仪器的名称:_______________。
③步骤Ⅲ生成SnO的离子方程式:__________________。
④步骤Ⅴ操作依次为 _____________、____________、过滤、洗涤、低温干燥。
(4)SnCl4蒸气遇氨及水汽呈浓烟状,因而可制作烟幕弹,其反应的化学方程式为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com