
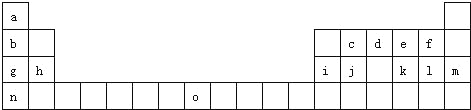
【题目】如表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.
试回答下列问题:

(1)请写出元素O的基态原子电子排布式 .
(2)c元素的一种同素异形体与熔融的n单质形成石墨间隙化合物,比较常见的石墨间隙化合物是青铜色的化合物,其化学式可写作CxK,其平面图形见图1,则x值为 .
(3)第三周期8种元素按单质熔点高低的顺序如图2,其中序号“8”代表 (填元素符号);其中电负性最大的是 (填右图中的序号).
(4)由i原子跟d原子以1:1相互交替结合而形成的晶体,晶型与晶体j相同.则i与d形成的晶体中一个晶胞中含有4个i原子;与同一个i原子相连的d原子构成的空间构型为 ,d原子的杂化类型为 .
(5)i单质晶体中原子的堆积方式如图3甲所示,其晶胞特征如图3乙所示,原子之间相互位置关系的平面图如图3丙所示.若已知i的原子半径为dcm,NA代表阿伏加德罗常数,i的相对原子质量为M,则该晶体的密度为 g/cm3(用字母表示).
【答案】(1)1s22s22p63s23p63d64s2;
(2)8;
(3)Si;2.
(4)正四面体;sp3;
(5)![]() .
.
【解析】
试题分析:根据元素周期表知,a﹣o各元素分别是H、Li、C、N、O、F、Na、Mg、Al、Si、S、Cl、Ar、K、Fe.
(1)Fe原子核外电子数为26,根据能量最低原理书写核外电子排布式;
(2)可以取三个钾原子形成的小三角形为计算单位,其完全占有的碳原子数是4,每个K为6个小三角形共用,利用均摊法计算K原子个数,据此解答;
(3)第三周期8种元素的单质中只有Si为原子晶体,熔沸点最大;
同周期随原子序数增大,电负性增大,故Cl元素电负性最大,氯气的沸点仅高于氩;
(3)AlN晶体与金刚石类似,每个Al原子与个N原子相连,为空间网状结构,与同一个Al原子相连的N原子构成正四面体;N原子成4个共价键(存在配位键),不含孤对电子,采取sp3杂化;
(5)利用均摊法计算晶胞中含有的原子个数,进而计算晶胞中含有原子的质量,Al的原子半径为dcm,由图丙可知,晶胞的棱长=4d cm×![]() =2
=2![]() d cm,再计算晶胞的体积,再根据密度公式计算其密度.
d cm,再计算晶胞的体积,再根据密度公式计算其密度.
解:(1)Fe原子核外电子数为26,根据能量最低原理可知,其核外电子排布式为:1s22s22p63s23p63d64s2,
故答案为:1s22s22p63s23p63d64s2;
(2)可以取三个钾原子形成的小三角形为计算单位,其完全占有的碳原子数是4,每个K为6个小三角形共用,占有的钾原子数为![]() ×3=
×3=![]() ,故碳原子数和钾原子数之比是4:
,故碳原子数和钾原子数之比是4:![]() =8:1,故x=8,
=8:1,故x=8,
故答案为:8;
(3)第三周期8种元素的单质中只有Si为原子晶体,熔沸点最大,由图可知序号“8”代表的为Si;同周期随原子序数增大,电负性增大,故Cl元素电负性最大,氯气的沸点仅高于氩,故序号“2”为Cl,
故答案为:Si;2.
(4)AlN晶体与金刚石类似,每个Al原子与个N原子相连,为空间网状结构,与同一个Al原子相连的N原子构成正四面体;N原子成4个共价键(存在配位键),不含孤对电子,采取sp3杂化,
故答案为:正四面体;sp3;
(5)由晶胞结构可知,晶胞中Al原子的数目为8×![]() +6×
+6×![]() =4,该晶胞中原子的质量=4×
=4,该晶胞中原子的质量=4×![]() g,由信息可知晶胞图可知为面心立方,Al的原子半径为dcm,由图丙可知,晶胞的棱长=4d cm×
g,由信息可知晶胞图可知为面心立方,Al的原子半径为dcm,由图丙可知,晶胞的棱长=4d cm×![]() =2
=2![]() d cm,故晶胞的体积=(2
d cm,故晶胞的体积=(2![]() d cm)3=16
d cm)3=16![]() d3cm3,所以其密度=
d3cm3,所以其密度=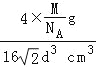 =
=![]() g/cm3,
g/cm3,
故答案为:![]() .
.


科目:高中化学 来源: 题型:
【题目】化学无处不在,下列与化学有关的说法错误的是
A.生活中常见金属镁、铝、铁、铜等均能通过热还原法冶炼
B.古方记载:“青蒿一捏,以水二升渍,绞其汁”,所述过程不涉及化学变化
C.绿色化学的核心是减少和消除工业生产对环境的污染
D.通过煤的干馏、气化、液化能获得多种化工原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学﹣﹣选修物质结构与性质]
下表为长式周期表的一部分,其中的序号代表对应的元素.

(1)写出上表中元素⑨原子的外围电子排布式 .
(2)在元素③与①形成的水果催熟剂气体化合物中,元素③的杂化方式为 杂化;元素⑦与⑧形成的化合物的晶体类型是 .
(3)元素④的第一电离能 > ⑤(填写“>”、“=”或“<”)的第一电离能;元素④与元素①形成的X分子的空间构型为 .请写出与元素④的单质互为等电子体分子、离子的化学式 (各写一种).
(4)在测定元素①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是 .
(5)④的最高价氧化物对应的水化物稀溶液与元素⑦的单质反应时,元素④被还原到最低价,该反应的化学方程式为 .
(6)将过量的X通入含有元素⑩的蓝色硫酸盐溶液中,反应的离子方程式为 ;元素⑩的某种氧化物的晶体结构如图所示,其中实心球表示元素⑩原子,则一个晶胞中所包含的氧原子数目为 .

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于常见有机物的说法正确的是
A.乙醚和乙醇互为同分异构体
B.糖类、油脂、蛋白质均能发生水解反应
C.聚氯乙烯可用作生产食品包装材料的原料
D.分子式为C3H8O的有机物,只有2种能发生酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,不正确的是
A.油脂水解的产物中一定含甘油
B.糖类、油脂和蛋白质都属于高分子化合物
C.氨基酸既能与盐酸反应,也能与NaOH反应
D.医疗上用75%的酒精消毒是因为其能使蛋白质变性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列有关0.1 mol·L-1醋酸溶液的说法中,正确的是
A.pH = 1
B.c(H+) = c(CH3COO-)
C.加入少量CH3COONa固体后,醋酸的电离程度减小
D.与0.1 mol·L-1 NaOH溶液等体积混合后所得溶液显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡: NH2COONH4(s)![]() 2NH3(g)+CO2(g)不能判断该分解反应已经达到化学平衡的是( )
2NH3(g)+CO2(g)不能判断该分解反应已经达到化学平衡的是( )
A. v(NH3)正= 2v(CO2)逆
B. 密闭容器中总压强不变
C. 密闭容器中氨气的体积分数不变
D. 密闭容器中混合气体的密度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法错误的是
A. 2,2-甲基丙烷也称新戊烷
B. 由乙烯生成乙醇属于加成反应
C. 分子式为C5H11Cl的有机物共有8种(不含立体异构)
D. 所有的糖类、油脂、蛋白质都可以发生水解反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com