
| A.1:4 | B.2:3 | C.6:5 | D.7:2 |
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源:不详 题型:单选题
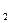 混合气体,在足量的氧气中燃烧,产物全部通过足量的Na
混合气体,在足量的氧气中燃烧,产物全部通过足量的Na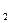 O
O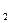 ,则Na
,则Na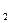 O
O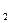 增重( )
增重( )| A.2 g | B.3?8 g |
| C.5 g | D.无法计算 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只有① | B.只有③ |
| C.①②③ | D.全部 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| 物 质 | 开始沉淀 | 沉淀完全 | 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)2 | 2.7 | 3.7 | Mn(OH)2 | 8.3 | 9.8 |
| Fe(OH)3 | 7.6 | 9.6 | Mg(OH)2 | 9.9 | 11.1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2 | B.CO | C.C12H22O11 | D.C6H12O6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
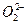 的过氧化物,下列叙述中不正确的是( )
的过氧化物,下列叙述中不正确的是( )| A.过氧化钡的化学式是BaO2 |
B.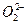 的电子式是[ 的电子式是[ ]2- ]2- |
| C.1 mol Na2O2或BaO2跟足量的水反应都生成0.5 mol O2 |
| D.过氧化钠和过氧化钡都是强氧化剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.观察样品外观 | B.在少量的样品中滴入几滴水 |
| C.在饱和溶液中滴入几滴酚酞 | D.取少量的试样加热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com