
| A. | 苹果放在空气中久置变黄和纸张久置变黄原理相似 | |
| B. | 高温或日常用的消毒剂可使禽流感病毒蛋白质变性 | |
| C. | 淘米水中含有淀粉可以直接检测加碘盐中是否含有碘元素 | |
| D. | 误食重金属盐引起人体中毒,可喝大量的食盐水解毒 |
分析 A.纸张久置变黄因为纸张纤维间的空隙中会渗入很多霉菌之类的真菌孢子,苹果久置变黄是因为所含二价铁离子被氧化生成三价铁离子;
B、根据蛋白质的理化性质和生理功能发生改变的现象称为蛋白质的变性;
C、加碘盐中加入的是碘的化合物,不是碘单质;
D、重金属盐,能够使蛋白质变性.
解答 解:A.纸张久置变黄因为纸张纤维间的空隙中会渗入很多霉菌之类的真菌孢子,苹果久置变黄是因为所含二价铁离子被氧化生成三价铁离子,二者原理不相同,故A错误;
B、根据蛋白质的理化性质和生理功能发生改变的现象称为蛋白质的变性.物理因素有:加热、加压、搅拌、振荡、紫外线照射、超声波等;化学因素有:强酸、强碱、重金属盐、三氯乙酸、乙醇、丙酮等,故高温或日常用的消毒剂可使禽流感病毒蛋白质变性,故B正确;
C、碘与淀粉变蓝是指与碘单质与淀粉变蓝,而不是碘的化合物,而食盐加碘加入的是碘的化合物,故C错误;
D、重金属盐,能够使蛋白质变性,引起人体中毒,可以服用牛奶或者鸡蛋清等解毒,故D错误.
故选B.
点评 本题主要考查有机物的性质、蛋白质的变性以及物质的检验等,难度较小,旨在考查学生对基础知识的识记,注意基础知识的积累掌握.


科目:高中化学 来源: 题型:解答题
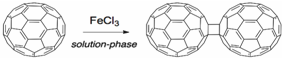

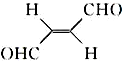 ,下列叙述正确的有AD.
,下列叙述正确的有AD.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室用Zn和稀硫酸制H2,为加快反应速率,可向稀硫酸中加入少量Cu粉 | |
| B. | CH3Cl(g)+Cl2(g)$\stackrel{光照}{→}$CH2Cl2(l)+HCl(g)常温下能自发进行,则该反应的△H>0 | |
| C. | 在一体积可变的恒温密闭容器中发生反应PCl3(g)+Cl2(g)?PCl5(g),压缩体积,平衡正向移动,K值增大 | |
| D. | 25℃时Ka(HClO)=3.0×10-8,Ka(HCN)=4.9×10-10,若该温度下NaClO溶液与NaCN溶液pH相同,则c(NaClO)<c(NaCN) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA | |
| B. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| C. | 常温常压下,3.2gO2和3.2gO3中所含氧原子数都是0.2NA | |
| D. | 将常温下含NA个NO2、N2O4分子的混合气体的温度降至标准状况,其体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷,丙烯 | B. | 乙烷,乙烯 | C. | 甲烷,乙烯 | D. | 乙烷,丙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化氮与氧气 | B. | 一氧化氮与二氧化氮 | ||
| C. | 硝酸与一氧化氮 | D. | 硝酸与水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
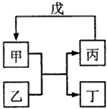 下列各组物质中,不满足如图所示转化关系的是(反应条件略去,箭头表示一步转化)
下列各组物质中,不满足如图所示转化关系的是(反应条件略去,箭头表示一步转化)| 甲 | 乙 | 丙 | 戊 | |
| A | NH3 | Cl2 | N2 | H2 |
| B | C | SiO2 | CO | CuO |
| C | Al(OH)3 | NaOH溶液 | NaAlO2溶液 | CO2 |
| D | 乙醇乙酯 | NaOH溶液 | 乙醇 | 乙酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com