
【题目】有一在空气中放置了一段时间的NaOH固体,经分析测知其含水7%,含Na2CO353%,其余为NaOH。取10克该样品恰好和100毫升2molL-1的盐酸反应,蒸发反应后的溶液可得到固体的质量为( )
A.5.85克B.10克C.17.55克D.11.7克
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.常温下NO2是无色气体,能与水发生反应
B.SiO2难溶于水,不能与NaOH溶液反应
C.浓硝酸能与铜反应生成H2
D.实验室常用NH4Cl和Ca(OH)2固体混合物加热来制取NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一.某研究小组进行如下实验:采用如图1装置(实验前已除尽装置内的空气)制取Na2S2O5 . 已知:①装置Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2═Na2S2O5 .
②Na2S2O5晶体在空气中被氧化生成Na2SO4 . 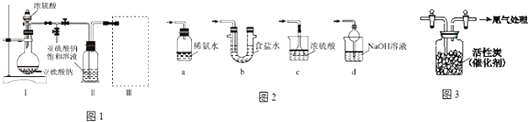
(1)装置Ⅰ中产生气体的化学方程式为 .
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是 .
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(图2)(夹持仪器已略去)为(填序号).
(4)检测Na2S2O5晶体在空气中已被氧化的实验方案是 .
(5)为了研究干燥的Cl2与干燥SO2反应及进行程度.用如图3所示装置收集满干燥的Cl2 , 再通入干燥SO2 , 集气瓶中立即产生无色液体SO2Cl2 , 充分反应后,将液体和剩余气体分离.继续用NaOH溶液吸收分离出的气体,用足量稀盐酸酸化后,再滴加BaCl2溶液,产生白色沉淀,该白色沉淀是 , 由此可知反应后剩余气必然存在气体,综合实验信息,请写出干燥的SO2与Cl2反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于气体摩尔体积的几种说法正确的是( )
A.22.4L任何气体的物质的量均为1mol
B.非标准状况下,1mol任何气体不可能占有22.4L体积
C.0.4molH2、0.2molO2、和0.4molCO2组成的混合气体,在标准状况下约为22.4L
D.同温、同压下,相同质量的CO和CO2具有相同的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某强氧化剂XO(OH)2+50mL2.4mol/L与30mL2mol/L的Na2SO3溶液恰好完全反应,则X还原后化合价为
A.+2B.+4C.0D.+6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2CO(g)+O2(g)=2CO2(g) △H=-566kJ/mol Na2O2(s)+CO2(g)=Na2CO3(s)+1/2O2(g) △H=-226kJ/mol。根据以上热化学方程式判断,下列说法正确的是
A. CO的燃烧热为-283kJ/mol
B. 右图可表示由CO生成CO2的反应过程和能量关系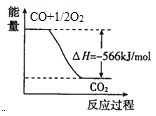
C. 2Na2O2(s)+2CO2(s)=Na2CO3(s)+O2(g) △H>-452kJ/mol
D. CO(g)与Na2O2(s)反应放出509kJ热量时,转移电子个数为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列小题.
(1)0.5mol NH3共含有个电子
(2)27.75g某+2价金属的氯化物(MCl2)中含有3.01×1023个Cl﹣ , 则M的相对原子量为
(3)如图是某化学实验室从化学试剂商店买回的盐酸试剂标签上的部分内容
①该浓盐酸的物质的量浓度
②用该浓盐酸配制200mL1mol/L的稀盐酸所需该浓盐酸的体积是mL(用量筒量取)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学无处不在,与化学有关的说法正确的是( )
A.我国自行研制的航母中使用到了大量特种钢,钢属于合金
B.珠三角是酸雨重灾区,酸雨主要成分是硝酸和碳酸
C.碘是人体必需微量元素,食盐加碘加的就是碘单质
D.节日里五颜六色的焰火利用的是金属单质的焰色反应,焰色反应属于化学变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com