
【题目】A、B、C、D均为中学化学常见物质,且含有一种相同的元素,它们之间有如下转化关系,其中A是单质。
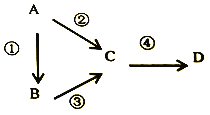
(1)若A是一种淡黄色固体,B是气态氢化物,C、D 为气态氧化物,且C是形成酸雨的主要物质。请写 出 C与 B反应的化学方程式_________。
(2)若B是气态氢化物,C、D为气态氧化物,且C、D是形成光化学烟雾的一个重要原因。请写出反应③的化学方程式_________。实验室中检验气体B存在用的试剂或用品为_________。
(3)若B、D既能溶于强酸溶液,又能溶于强碱瑢液,反应②③均需要强碱性溶液,反应④可以通过滴加少量稀盐酸实现。据此判断A元素在周期表中的位置是_________。请写出②的离子方程式_________。
(4)若C是一种淡黄色固体,常用于呼吸面具中的供氧剂,D是一种强碱。写出反应 ④的离子方程式_________。
【答案】 2H2S+SO2=3S+2H2O 4NH3+5O2![]() 4NO+6H2O 湿润的红色石蕊试纸 第3周期第ⅢA族 2A1+2OH-+6H2O=2[A1(OH)4]- +3H2↑ 2Na2O2+2H2O=4Na++4OH-+O2↑
4NO+6H2O 湿润的红色石蕊试纸 第3周期第ⅢA族 2A1+2OH-+6H2O=2[A1(OH)4]- +3H2↑ 2Na2O2+2H2O=4Na++4OH-+O2↑
【解析】试题分析:(1)若A是一种淡黄色固体,B是气态氢化物,C、D为气态氧化物,且C是形成酸雨的主要物质,则符合条件的应该是A是S,B是H2S,C是SO2,D是SO3。
(2)若B是气态氢化物,C、D为气态氧化物,且C、D是形成光化学烟雾的一个重要原因,这说明是氮元素及其化合物的转化,因此A是氮气,B是氨气,C是NO,D是NO2。
(3)若B、D既能溶于强酸溶液,又能溶于强碱溶液,反应②③均需要强碱性溶液,反应④可以通过滴加少量稀盐酸实现,这说明该转化是铝及其化合物的转化,因此符合条件的是A是Al,B是氧化铝,C是偏铝酸钠,D是氢氧化铝。
(4)若C是一种淡黄色固体,常用于吸吸面具中的供氧剂,D是一种强碱,因此C是过氧化钠,D是氢氧化钠。
解析:根据以上分析,(1) H2S具有还原性,SO2具有氧化性,二者可以发生氧化还原反应生成单质硫和水,反应的化学方程式为2H2S+SO2=3S+2H2O。
(2)氨气发生催化氧化生成NO和水,所以反应③的化学方程式为4NH3+5O2![]() 4NO+6H2O。氨气是碱性气体能使湿润的红色石蕊试纸变蓝色,所以可以用湿润的红色石蕊试纸检验氨气。
4NO+6H2O。氨气是碱性气体能使湿润的红色石蕊试纸变蓝色,所以可以用湿润的红色石蕊试纸检验氨气。
(3) Al元素在周期表中的位置是第三周期第ⅢA族。金属铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,因此②的离子方程式为2Al+2OH-+6H2O=[Al(OH)4]-+3H2↑。
(4)过氧化钠溶于水即生成氢氧化钠和氧气,所以反应④的离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】下列表述或化学用语书写正确的是
A. 向Ba(OH)2溶液中滴加NaHSO4溶液至混合溶液恰好为中性:Ba2+ +OH-+H++SO42-=BaSO4↓+H2O
B. 稀硫酸中加入铁粉:2Fe+6H+=2Fe3++3H2↑
C. FeSO4溶液与稀硫酸、双氧水混合:2Fe2++H2O2+2H+=2Fe3++2H2O
D. 金属铝与氧化镁发生铝热反应:2Al+3MgO![]() 3Mg+Al2O3
3Mg+Al2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种化学性质活泼的气体。(1)新制备的氯水呈浅黄绿色,说明氯水中有 分子存在(写化学式)。向氯水中滴入几滴AgNO3溶液,现象是 。
(2)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察的现象是 。

(3)为防止氯气污染空气,可用 溶液吸收多余的氯气,该反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关晶体的结构如下图所示,下列说法中不正确的是


A. 在NaCl晶体中,距Na+最近的Cl-形成正八面体
B. 在CaF2晶体中,每个晶胞平均占有4个Ca2+
C. 在金刚石晶体中,6个碳原子形成一个环且不在同一平面上
D. 该气态团簇分子的分子式为EF或FE
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于强弱电解质及非电解质的组合完全正确的是( )
A | B | C | D | |
强电解质 | NaCl | H2SO4 | NaOH | HNO3 |
弱电解质 | HF | BaSO4 | CaCO3 | CH3COOH |
非电解质 | Cl2 | CO2 | C2H5OH | SO2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,室温下分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的1/4)、H2 和O2 的混合气体,若将H2、O2 的混合气体点燃引爆。活塞先左弹,恢复室温后,活塞右滑停留于容器的中央。则原来H2、O2 的物质的量之比可能为①4∶5 ② 2∶5 ③3∶8 ④7∶2

A. ①② B. ①④ C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,生成的沉淀质量与滴入NaOH溶液体积关系如图,则原混合溶液中MgCl2与FeCl3的物质的量之比为

A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物与人类生产、生活息息相关。 回答下列问题:
(1)前4周期元素中,基态原子核外电子排布成单电子数最多的元素的价层电子排布式为________________。
(2)N2F2分子中氮原子的杂化方式是_________,1molN2F2含有______mol σ键。
(3)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1molNH4BF4含有___________mol配位键。
(4)MgO、CaO两种晶体的结构与NaCl晶体结构相似,则两种离子晶体的熔点大小关系为 _____>_____(用化学式表示),![]() 的沸点比
的沸点比 ____(填“高”或“低”);原因是______________________。
____(填“高”或“低”);原因是______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com