
| A.①④ | B.①③ | C.①③④ | D.② |
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
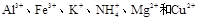 等离子中的一种或几种。现加入Na2O2粉末只有无色无味的气体放出,并同时析出白色沉淀。如加入Na2O2的量与生成白色沉淀的量之间的关系用下图来表示。
等离子中的一种或几种。现加入Na2O2粉末只有无色无味的气体放出,并同时析出白色沉淀。如加入Na2O2的量与生成白色沉淀的量之间的关系用下图来表示。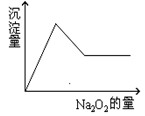
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
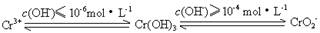
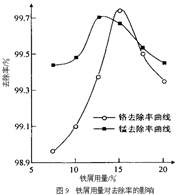
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
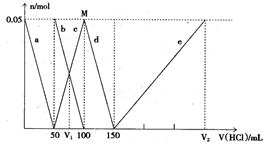
| A.原混合溶液中的CO32-与AlO2—的物质的量之比为1:2 |
| B.V1:V2=l:5 |
| C.M点时生成的CO2为0、05mol |
| D.a曲线表示的离子方程式为:AlO2—+H++H2O=Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
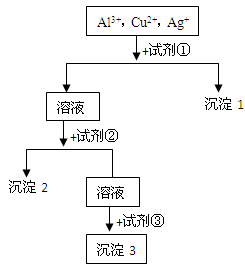
 ⑴各取适量固体试剂分别加入5支试管中,
⑴各取适量固体试剂分别加入5支试管中, 加入适量蒸馏水,振荡试管,观察则 被检出的物质的化学式是
加入适量蒸馏水,振荡试管,观察则 被检出的物质的化学式是  ⑵分别取未检出液,往其中加入上述已检出的溶液,观察到的现象和相应的离子方程式:
⑵分别取未检出液,往其中加入上述已检出的溶液,观察到的现象和相应的离子方程式: ①现象:试管中有白色沉淀生成,离子方程式: ;
①现象:试管中有白色沉淀生成,离子方程式: ; ②现象:试管中有蓝色沉淀生成,离子方程式: ;
②现象:试管中有蓝色沉淀生成,离子方程式: ;查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.Cl- | B.NO3- | C.CO32- | D.OH- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.HCO3— | B.Na+ | C.Ba2+ | D.NO3— |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com