
| A. | 热稳定性:H2Se>H2S>H2O | B. | 原子半径:Se>Cl>S | ||
| C. | 酸性:H2SeO4<H2SO4<HClO4 | D. | 还原性:S2->Se2->Br- |
分析 A.元素非金属性越强,其氢化物的稳定性越强;
B.电子层数越多原子半径越大,同一周期元素原子半径随着原子序数增大而减小;
C.元素非金属性越强,其最高价氧化物的水化物酸性越强;
D.元素非金属性越强,其简单阴离子还原性越弱.
解答 解:A.元素非金属性越强,其氢化物的稳定性越强,非金属性O>S>Se,所以氢化物的稳定性H2Se<H2S<H2O,故A错误;
B.电子层数越多原子半径越大,同一周期元素原子半径随着原子序数增大而减小,Se有四个电子层、S和Cl有三个电子层,且S原子序数小于Cl,所以原子半径Se>S>Cl,故B错误;
C.元素非金属性越强,其最高价氧化物的水化物酸性越强,非金属性Cl>S>Se,所以最高价氧化物的水化物酸性H2SeO4<H2SO4<HClO4,故C正确;
D.元素非金属性越强,其简单阴离子还原性越弱,非金属性Br>S>Se,所以还原性:Se2->S2->Br-,故D错误;
故选C.
点评 本题考查同一周期同一主族元素性质递变规律,为高频考点,明确元素周期律内涵是解本题关键,知道非金属性强弱判断方法,题目难度中等.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 不变 | B. | 增大 | C. | 减少 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应是置换反应 | |
| B. | 该反应只有K2FeO4为氧化产物 | |
| C. | 3mol氯气参与反应转移电子数为6个 | |
| D. | 该反应条件下K2FeO4的氧化性大于Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
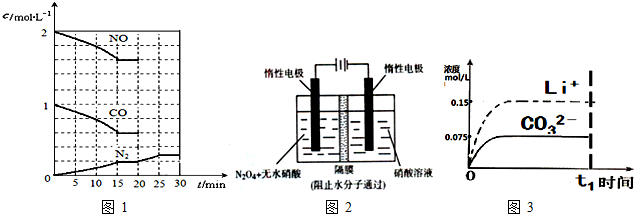 (填“向左”、“向右”或“不”).
(填“向左”、“向右”或“不”).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2中混有HCl,可依次通入盛有饱和食盐水、浓H2SO4的洗气瓶 | |
| B. | NH4Cl 溶液中混有Fe3+,可加入NaOH溶液后过滤 | |
| C. | CO中混有CO2,可依次通入盛NaOH 溶液、浓 H2SO4的洗气瓶 | |
| D. | Na2CO3固体中混有NaHCO3,可用灼烧的方法除尽 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2是酸性氧化物,能与NaOH溶液反应 | |
| B. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| C. | 硫化亚铁溶于稀硝酸中的离子方程式为:FeS+2H+═Fe2++H2S↑ | |
| D. | pH=1的溶液中:Fe2+、NO3-、SO42-、Na+能够大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑤ | B. | ①②③ | C. | ②③④⑥ | D. | ①③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com