
分析 现有一份含有FeCl3和FeCl2固体的混合物,为测定FeCl2的含量,
①称取混合物样品的质量7.06g,将样品溶解,溶解过程中需要加入稀盐酸抑制氯化铁、氯化亚铁水解,避免生成沉淀;
②向溶解后的溶液中,加入足量的双氧水,是氧化亚铁离子为铁离子,
③再向②所得溶液中加入足量的NaOH溶液,得到红褐色沉淀氢氧化铁,
④将沉淀过滤、洗涤后,加热灼烧,到质量不再减少,得到固体物质4.00g为氧化铁,结合铁元素守恒和质量关系列式计算得到氯化亚铁质量,计算得到氯化亚铁含量;
(1)样品溶解过程中需加入稀盐酸,主要是抑制氯化铁、氯化亚铁水解;
(2)酸性溶液中过氧化氢氧化亚铁离子为铁离子;
(3)过滤操作过程、装置选择所需玻璃仪器;
(4)简述检验实验步骤④中沉淀已经洗涤干净的方法是滴加硝酸酸化的硝酸银溶液检验洗涤液中是否含氯离子;
(5)设原FeCl3和FeCl2固体的混合物中氯化亚铁物质的量为x,氯化铁物质的量为y,
127x+162.5y=7.06
x+y=$\frac{4.0g}{160g/mol}$×2
计算得到氯化亚铁质量分数;
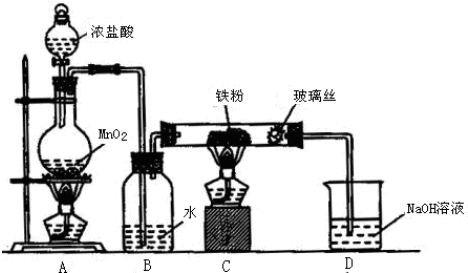
(6)氯化铁易吸收水蒸气,通过装置B中水吸收氯化氢,得到氯气中混有水蒸气,进入装置C,会使生成的氯化铁潮解,氢氧化钠溶液中水蒸气也会进入装置C影响产物的纯度.
解答 解:现有一份含有FeCl3和FeCl2固体的混合物,为测定FeCl2的含量,
①称取混合物样品的质量7.06g,将样品溶解,溶解过程中需要加入稀盐酸抑制氯化铁、氯化亚铁水解,避免生成沉淀;
②向溶解后的溶液中,加入足量的双氧水,是氧化亚铁离子为铁离子,
③再向②所得溶液中加入足量的NaOH溶液,得到红褐色沉淀氢氧化铁,
④将沉淀过滤、洗涤后,加热灼烧,到质量不再减少,得到固体物质4.00g为氧化铁,结合铁元素守恒和质量关系列式计算得到氯化亚铁质量,计算得到氯化亚铁含量.
(1)上述分析可知样品溶解过程中需加入稀盐酸,主要是抑制氯化铁、氯化亚铁水解,防止溶解过程中生成沉淀使溶液变浑浊,
故答案为:稀盐酸;FeCl3和 FeCl2水解而使溶液浑浊;
(2)酸性溶液中过氧化氢氧化亚铁离子为铁离子,反应的离子方程式为:2Fe2++2H++H2O2=2Fe3++2H2O,
故答案为:2Fe2++2H++H2O2=2Fe3++2H2O;
(3)过滤操作过程、装置选择所需玻璃仪器为漏斗、玻璃棒、烧杯,过滤操作中除用漏斗外,还需要的玻璃仪器有玻璃棒、烧杯,
故答案为:玻璃棒、烧杯;
(4)检验实验步骤④中沉淀已经洗涤干净的方法是滴加硝酸酸化的硝酸银溶液检验洗涤液中是否含氯离子,具体步骤为:取最后的洗涤液少量,滴加硝酸酸化的硝酸银溶液,如果没有白色沉淀生成,说明沉淀已经洗涤干净,
故答案为:取最后的洗涤液少量,滴加硝酸酸化的硝酸银溶液,如果没有白色沉淀生成,说明沉淀已经洗涤干净;
(5)设原FeCl3和FeCl2固体的混合物中氯化亚铁物质的量为x,氯化铁物质的量为y,
127x+162.5y=7.06
x+y=$\frac{4.0g}{160g/mol}$×2
x=0.03mol
y=0.02mol
计算得到氯化亚铁质量分数=$\frac{0.03mol×127g/mol}{7.06g}$×100%=53.97%,
故答案为:53.97%;
(6)装置A是制备氯气装置,生成的氯气中含水蒸气、氯化氢,通过装置B中水吸收氯化氢,得到氯气中混有水蒸气,进入装置C,会使生成的氯化铁潮解,剩余氯气被氢氧化钠溶液吸收,防止污染空气,装置BC和装置CD间都会导致水蒸气进入装置C,氯化铁易吸收水蒸气发生潮解,所以在 B、C 之间和C、D之间分别增加盛有浓硫酸的洗气瓶,防止 FeCl3吸水而潮解,
故答案为:在 B、C 之间和C、D之间分别增加盛有浓硫酸的洗气瓶,防止 FeCl3吸水而潮解.
点评 本题考查了物质组成的实验测定方法、过程分析判断、含量的计算应用等知识点,注意实验中的注意问题和基本操作掌握,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:推断题
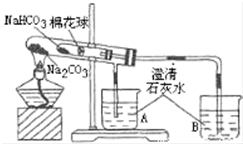 某小组同学通过对比实验了解Na2CO3和NaHCO3性质的异同,如表是他们撰写的实验报告的一部分.
某小组同学通过对比实验了解Na2CO3和NaHCO3性质的异同,如表是他们撰写的实验报告的一部分. | 实验序号 | 实验步骤(内容) | 现象 |
| ① | 在贴有标签a、b的试管中分别加入1.0gNa2CO3固体和NaHCO3固体,观察外观. | / |
| ② | 继续向两试管中分别加入10.0mL水,用力振荡,观察现象. | / |
| ③ | 再分别向两试管中滴加2滴酚酞溶液,观察现象. | 溶液变红 |
| ④ | 加热大试管一段时间.(注:棉花球沾有无水硫酸铜粉末) | 有无水硫酸铜粉末的棉花球变蓝,A烧杯中没有明显现象,B烧杯中有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
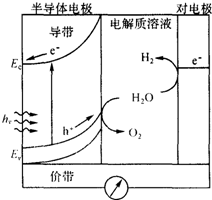 太阳能发电和阳光分解水制氢气,是清洁能源研究的主攻方向,研究工作之一集中在n-型半导体光电化学电池方面.如图是n-型半导体光电化学电池光解水制氢的基本原理示意图,图中的半导体导带是未充填电子的能级最低的能带,半导体价带是已充填价电子的能级最高的能带,图中的e-为电子、h+为空穴.在光照下,电子(e-)由价带跃迁到导带后,然后流向对电极.下列说法不正确的是( )
太阳能发电和阳光分解水制氢气,是清洁能源研究的主攻方向,研究工作之一集中在n-型半导体光电化学电池方面.如图是n-型半导体光电化学电池光解水制氢的基本原理示意图,图中的半导体导带是未充填电子的能级最低的能带,半导体价带是已充填价电子的能级最高的能带,图中的e-为电子、h+为空穴.在光照下,电子(e-)由价带跃迁到导带后,然后流向对电极.下列说法不正确的是( )| A. | 对电极表面发生的电极反应式为:4H++4e-→2H2 | |
| B. | 电池的总反应式为:2H2O$\stackrel{hv}{→}$O2+2H2↑ | |
| C. | 整个过程中实现了太阳能向电能化学能等的转化 | |
| D. | 装置中电流的方向是从半导体电极流向对电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
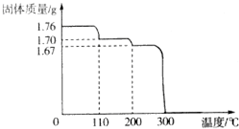 将1.76gHIO3固体样品放在热重分析仪中进行热重分析,测得其热重分析曲线(样品质量随温度变化的曲线)如图所示:
将1.76gHIO3固体样品放在热重分析仪中进行热重分析,测得其热重分析曲线(样品质量随温度变化的曲线)如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu是氧化剂 | B. | H2SO4在反应中只表现氧化性 | ||
| C. | Cu在反应中被氧化 | D. | 1mol氧化剂在反应中得到1mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 体积相等时具有的质量相等 | B. | 分子数相等时具有的中子数相等 | ||
| C. | 质量相等时具有的质子数相等 | D. | 体积相等时具有的原子数相等 |
查看答案和解析>>
科目:高中化学 来源:2017届江苏省如皋市高三上学期质量调研一化学试卷(解析版) 题型:选择题
硫酸钙可用于生产硫酸、漂白粉等一系列物质(见下图)。下列说法正确的是
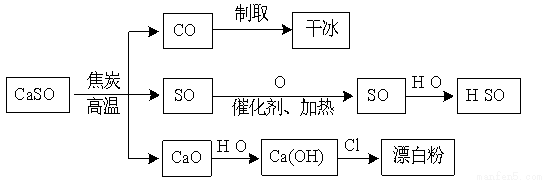
A.CO2制取干冰的过程吸收热量,属于物理变化
B.硫酸钙与焦炭反应时生成的n(CO2):n(SO2)=1:2
C.由SO2制取H2SO4的过程均为氧化还原反应
D.石灰乳与Cl2反应制取漂白粉时,Cl2仅作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验编号 | HA物质的量浓度(mol/L) | NaOH物质的量浓度(mol/L) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com