
铝合金在日常生活、建筑装潢、航空航天和汽车制造等方面均有着广泛的用途。下列关于铝合金具有广泛用途的分析不正确的是
A.铝元素在地壳中的含量高,储量丰富
B.铝容易形成致密的氧化膜,抗腐蚀性能好
C.铝化学性质稳定,常温下不与任何酸碱反应
D.铝的冶炼技术基本成熟,可以大量生产
 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:
铝土矿的主要成分为氧化铝、氧化铁和二氧化硅,工业上经过下列工艺可以冶炼金属铝:


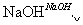
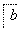 ,③F
,③F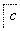 ,④F
,④F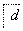


下列说法中错误的是
A.①②中除加试剂外,还需要进行过滤操作
B.a、b中铝元素的化合价相同
C.③中需要通入过量的氨气
D.④进行的操作是加热,而且d一定是氧化铝
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.铅蓄电池放电时铅电极发生氧化反应
B.电解饱和食盐水在阳极得到氯气,阴极得到金属钠
C.给铁钉镀铜可采用CuSO4作电镀液
D.生铁浸泡在食盐水中发生析氢腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
向四个体积相同的密闭容器中分别充入一定量的SO2和O2,开始反应时,按正反应速率由大到小的顺序排列正确的是( )
甲.在500 ℃时,SO2和O2各10 mol反应
乙.在500 ℃时,用V2O5作催化剂,10 mol SO2和10 mol O2起反应
丙.在450 ℃时,8 mol SO2和5 mol O2反应
丁.在500 ℃时,8 mol SO2和5 mol O2反应
A、甲、乙、丙、丁
B、乙、甲、丙、丁
C、乙、甲、丁、丙
D、丁、丙、乙、甲
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸是一种重要的化工产品,硫酸的消耗量常被视为一个国家工业发达水平的一种标志。目前的重要生产方法是“接触法”,有关接触氧化反应2SO2+O2催化剂2SO3的说法不正确的是( )
A、该反应为可逆反应,故在一定条件下二氧化硫和氧气不可能全部转化为三氧化硫
B、达到平衡后,反应就停止了,故正、逆反应速率相等且均为零
C、一定条件下,向某密闭容器中加入2molSO2和1molO2,则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等
D、在利用上述反应生产三氧化硫时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题
查看答案和解析>>
科目:高中化学 来源: 题型:
类推的思维方法在化学学习与研究中有时会产生错误结论,因此类推的结论最终要经过实践的检验,才能决定其正确与否,下列几种类推结论中,错误的是
①钠与水反应生成NaOH和H2;所有金属与水反应都生成碱和H2
②铁露置在空气中一段时间后就会生锈;性质更活泼的铝不能稳定存在于空气中
③化合物NaCl的焰色为黄色;Na2CO3的焰色也为黄色
④密度为1.1 g·cm-3与密度为1.2 g·cm-3的NaCl溶液等体积混合,所得NaCl溶液的密度介于1.1 g·cm-3与1.2 g·cm-3之间,Na-K合金的熔点应介于Na和K熔点之间
A.①② B.①④ C.①②③④ D.①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
小王喜欢做实验,一次他将一把没有擦干的小刀放在火上烤了一下,发现表面变蓝,他又将一把干燥的光亮小刀放 在火上烤了一下,发现也有同样的现象发生,他分析后认为可能是火烤的过程中小刀表面生成了一种物质所造成的。你认为此物质最有可能是
A.Fe3O4 B.FeO C.Fe2O3 D.Fe(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法正确的是
A.常温常压下,14g由N2与CO组成的混合气体含有的原子数目为2NA
B.1L 1mol·L-1的NaClO 溶液中含有ClO-的数目为NA
C.质量a g的C2H4和C3H6的混合物中共用电子对数目为3a NA /14
D.常温下,pH=13的NaOH溶液中含有OH一的数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
在冶金工业上,均不能用化学还原剂制得的一组金属是
A.Na、Mg、Al B.Na、K、Zn、Fe
C.Zn、Fe、Cu、Ag D.Mg、Al、Zn、Fe
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com