
 A、B、C、D为单质,其余均为化合物,已知A、B均能与X溶液反应生成气体D,C与D能化合成Y,X、Y都是常用试剂,反应③是化工工业生产的化学原理.它们之间具有如下图相互转化关系:
A、B、C、D为单质,其余均为化合物,已知A、B均能与X溶液反应生成气体D,C与D能化合成Y,X、Y都是常用试剂,反应③是化工工业生产的化学原理.它们之间具有如下图相互转化关系:
| ||
| ||
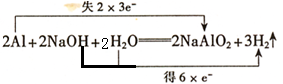 ,
,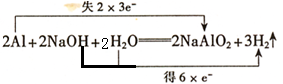 ;
;

 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:
| Ⅰ | Ⅱ | |
| A | Ba(OH)2溶液与过量NaHCO3 溶液混合 |
NaOH溶液与过量NaHCO3溶液 混合 |
| B | 少量SO2通入Ba(OH)2溶液中 | 过量SO2通入Ba(OH)2溶液中 |
| C | BaCl2溶液与Na2SO3溶液混合 | Ba(NO3)2溶液与H2SO3溶液混合 |
| D | 少量氨水滴入AlCl3溶液中 | 少量AlCl3溶液滴入氨水中 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al13和Al14互为同位素 |
| B、Al13和Al14“超级原子”内原子间通过离子键结合 |
| C、All4容易失去2个电子而形成稳定的All42+ |
| D、Al13具有较强的还原性,容易失去电子而形成阳离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:
 非金属单质A经如图所示的过程转化为含氧酸D.
非金属单质A经如图所示的过程转化为含氧酸D.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com