
【题目】以下流程是合成环烷烃的方法之一。
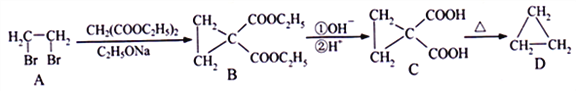
(1)B、C中含氧官能团的名称分别为____________、_______________。
(2)A→B的反应类型是____________。
(3)写出C→D反应的化学方程式__________________________________。
(4)写出同时满足下列条件的B的一种同分异构体的结构简式:____________
①分子中含三元环; ②分子中无甲基;③有4种不同化学环境的氢;④可发生银镜反应。
(5)请以1,3-丁二烯和CH2(COOC2H5)2、C2H5ONa为原料制备![]() ,写出相应的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。
,写出相应的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:

回答下列问题:
(1)NaClO2中Cl的化合价为_______。
(2)写出“反应”步骤中生成ClO2的化学方程式__________________________________。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去Mg2+和Ca2+,要加入的试剂分别为________、________。“电解”中阴极反应的主要产物是______。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2。此吸收反应中,氧化剂与还原剂的物质的量之比为________,该反应中氧化产物是_________。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。NaClO2的有效氯含量为____。(计算结果保留两位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据最新《参考消息》报道,有科学家提出硅是“21世纪的能源”、“未来的石油”的观点。假如硅作为一种普遍适用的新型能源被开发利用,关于其有利因素的下列说法中,你认为不妥的是()
A. 硅便于运输、贮存,从安全的角度考虑,硅是最安全的燃料
B. 自然界中存在大量的单质硅
C. 硅燃烧放出的热量多,且燃烧产物对环境污染程度低,容易有效控制
D. 自然界中硅易开采,且可再生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 1 mol CO2 的质量为44g/mol
B. CO2的摩尔质量为44g
C. CO2的摩尔质量等于CO2的相对分子质量
D. NA个CO2的质量与CO2的相对分子质量在数值上相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“温室效应”是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体,CO2的综合利用是解决温室及能源问题的有效途径。
(1)研究表明CO2和H2在催化剂存在下可发生反应生成CH3OH。己知部分反应的热化学方程式如下:
CH3OH(g)+![]() O2(g) = CO2(g)+2H2O(1) △H1=akJmol-1
O2(g) = CO2(g)+2H2O(1) △H1=akJmol-1
H2(g)+![]() O2(g) = H2O(1) △H2=bkJmol-1
O2(g) = H2O(1) △H2=bkJmol-1
H2O(g) = H2O(l) △H3=ckJmol-1
则 CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=__________kJmol-1
CH3OH(g)+H2O(g) △H=__________kJmol-1
(2)CO2催化加氢也能合成低碳烯烃: 2CO2(g)+6H2(g)![]() C2H4(g)+4 H2O (g),不同温度下平衡时的四种气态物质的物质的量如图1所示,曲线b表示的物质为_______________ (写化学式)。
C2H4(g)+4 H2O (g),不同温度下平衡时的四种气态物质的物质的量如图1所示,曲线b表示的物质为_______________ (写化学式)。

(3)CO2和H2在催化剂Cu/ZnO作用下可发生两个平行反应,分别生成CH3OH和CO。
反应 A:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
反应B:CO2(g)+ H2(g)![]() CO(g)+H2O(g)
CO(g)+H2O(g)
控制CO2和H2初始投料比为1∶3时,温度对CO2平衡转化率及甲醇和CO产率的影响如图2所示。

① 由图2可知温度升高CO的产率上升,其主要原因可能是__________________。
② 由图2可知获取CH3OH最适宜的温度是________________,下列措施有利于提高CO2转化为CH3OH的平衡转化率的措施有__________________。
A.使用催化剂 B.增大体系压强
C.增大CO2和H2的初始投料比 D.投料比不变和容器体积不变,增加反应物的浓度
(4)在催化剂表面通过施加电压可将溶解在水中的二氧化碳直接转化为乙醇,则生成乙醇的电极反应式为______________________________________________________。
(5)由CO2制取C的太阳能工艺如图3所示。“热分解系统”发生的反应为:2Fe3O4![]() 6FeO+O2↑,每分解1mol Fe3O4转移电子的物质的量为_____________;“重整系统”发生反应的化学方程式为_____________________________________________。
6FeO+O2↑,每分解1mol Fe3O4转移电子的物质的量为_____________;“重整系统”发生反应的化学方程式为_____________________________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 铅蓄电池在充电过程中,阴极得到电子质量增加
B. 1 mol羟基含电子数约为7×6.02×1023
C. 0.1 molL-1 CH3COOH溶液加水稀释后,溶液中![]() 的值减小
的值减小
D. Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把1 mol X气体和0.5 mol Y气体混合于2 L密闭容器中,发生如下反应:3X(g)+Y(g)![]() nZ(g)+2W(g),2 min末生成0.4 mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol/(L·min) ,试计算(写出计算过程)
nZ(g)+2W(g),2 min末生成0.4 mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol/(L·min) ,试计算(写出计算过程)
(1)前2 min内,用X表示的平均反应速率。_____
(2)2 min末时Y的转化率。_____
(3)化学方程式中Z的化学计量数n。_____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com