
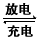 Li2S2O4�����йظõ�ص�˵����ȷ����___��
Li2S2O4�����йظõ�ص�˵����ȷ����___�� 
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ⷨ | B���Ȼ�ԭ�� | C���ȷֽⷨ | D��Ǧ�ȷ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ܶ���С�Ľ��� | B�����O2��Ӧ�����ƾ��ң�����Li2O | C��LiOH�ļ��Ա�NaOHǿ | D�������Ȼ��ʱ��������Ϻ�ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012���˽̰���л�ѧ����4.1 �������ý�������ͺ�ˮ��Դ��ϰ���������棩 ���ͣ�ѡ����
��������ܶ���С�Ľ������������Ľ�����﮿����ͷų�����ĵ��ӣ��ʳ�������������ܵ�ء���֪﮵Ľ����Խ����ƺ�þ֮�䣬��ұ�������Ӧ���õķ�����(����)
A����ⷨ B���Ȼ�ԭ�� C���ȷֽⷨ D�����ȷ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�����ɹŸ�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��������ܶ���С�Ľ������������Ľ�������ͷų�����ĵ��ӣ��ʳ����������������ء���֪﮵Ľ����Խ����ƺ�þ֮�䣬��������ұ��������﮵ķ�����(����)
A����ⷨ B���Ȼ�ԭ�� C���ȷֽⷨ D�����ȷ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com