
| A. | FeCl2 | B. | CuCl2 | C. | HCl | D. | FeCl3 |
科目:高中化学 来源: 题型:选择题
| A. | 丁达尔现象是用于鉴别胶体与溶液的方法 | |
| B. | 豆浆制豆腐是利用了胶体聚沉的原理 | |
| C. | 通电时氢氧化铁胶体微粒向直流电源正极移动 | |
| D. | 分散质微粒直径介于1~100mm之间的分散系称为胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 有A、D、E、G、M、L六种前四周期的元素.A元素的单质,是最轻的气体,D原子核外电子有11运动状态,E的负一价离子的核外3p轨道全充满.G原子的2p轨道有2个未成对电子,短周期元素M原子与G原子具有相同的价层电子排布.L位于周期表第12纵行且是六种元素中原子序数最大的.下图是由M、L形成的化合物R,其晶胞结构如图所示.
有A、D、E、G、M、L六种前四周期的元素.A元素的单质,是最轻的气体,D原子核外电子有11运动状态,E的负一价离子的核外3p轨道全充满.G原子的2p轨道有2个未成对电子,短周期元素M原子与G原子具有相同的价层电子排布.L位于周期表第12纵行且是六种元素中原子序数最大的.下图是由M、L形成的化合物R,其晶胞结构如图所示.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeO不稳定,在空气中加热迅速被氧化成Fe2O3 | |
| B. | 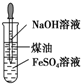 由图示操作可制取Fe(OH)2 | |
| C. | Fe3O4、Fe(OH)3都可以由化合反应制得 | |
| D. | Fe(OH)3胶体呈红褐色、透明,能发生丁达尔现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com