
分析 利用置换反应Zn+H2SO4=ZnSO4+H2↑,据此设计原电池时,锌为负极,铜为正极,工作时,正极反应式为2H++2e-=H2↑,负极反应式为Zn-2e-=Zn2+,Zn逐渐溶解,据此分析解答.
解答 解:(1)利用反应Zn+H2SO4=ZnSO4+H2↑设计原电池时,根据反应可知,Zn为负极,则正极可以是活泼性不如Zn的金属如Cu等,也可以是碳棒,电解质溶液是稀硫酸,
故答案为:铜片;锌片;
(2)正极上氢离子导致发生还原反应生成氢气,所以正极反应式为2H++2e-=H2↑,故答案为:2H++2e-=H2↑;
(3)负极是Zn、Cu是正极,电解质溶液是稀硫酸,所以装置图为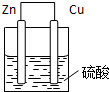 ,
,
实验现象:负极不断溶解,正极上气泡产生
由此得出的结论是:金属活动性Zn>Cu,
故答案为: ;金属活动性Zn>Cu.
;金属活动性Zn>Cu.
点评 本题考查原电池设计,为高频考点,根据元素化合价变化确定正负极材料及电解质溶液,一般来说,失电子发生氧化反应的金属作负极,发生还原反应的电解质为原电池电解质,题目难度不大.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:选择题
| A. | 氢气能还原氧化铜中的铜,铜能还原硝酸银溶液中的银,所以,氢气也能还原硝酸银溶液产生金属银 | |
| B. | CO2与SiO2化学式相似,故CO2与SiO2的结构、性质也相似 | |
| C. | 由“2Fe+3Cl2=2FeCl3”反应可推出“2Fe+3I2=2FeI3”反应也能发生 | |
| D. | K与Na同主族并位于Na的下方,Na常温下能与水剧烈反应,故K常温下也能与水剧烈反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+═AgBr | |
| B. | 乙醛溶液中加入足量的银氨溶液并加热CH3CHO+2$Ag(N{H}_{3}{)_{2}}^{+}$$\stackrel{水溶加热}{→}$$C{H}_{3}CO{O}^{-}$+$N{H}_{4}^{+}$+3NH3+2Ag↓+H2O | |
| C. | 向苯酚钠溶液中通入少量二氧化碳CO2+H2O+2C6H5O-→2C6H5OH+CO32- | |
| D. | 实验室用浓溴水检验苯酚: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M2+>X2+>Z2+>Y2+ | B. | X2+>M2+>Y2+>Z2+ | C. | Y2+>Z2+>M2+>X2+ | D. | Z2+>X2+>M2+>Y2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用A表示的反应速率是0.4mol/(L•min) | |
| B. | 分别用B、C、D表示的反应速率其比值是3:2:1 | |
| C. | 2min末时的反应速率,用B表示是0.3mol/(L•min) | |
| D. | υB=0.3mol/(L•min)和υC=0.2mol/(L•min),都表示该反应在这一时间内的反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 药品柜的同一层不可存放浓硝酸和浓氨水 | |
| B. | 保存在无色玻璃试剂瓶中的浓硝酸要放在阴凉处 | |
| C. | 铵态氮肥可与草木灰混合雨天施用 | |
| D. | 固氮就是将氮元素转化成固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可以按下面的框图进行反应.又知E溶液是无色的.
室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可以按下面的框图进行反应.又知E溶液是无色的.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com