
| 周期 族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | O |
| 一 | A | |||||||
| 二 | D | E | G | I | ||||
| 三 | B | C | F | H |


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
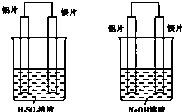 有甲和乙两位同学均想利用原电池反应来检测金属的活动性顺序,两人都使用镁片和铝片作电极,但甲同学将电极放到6mol?L-1 H2SO4溶液中,乙同学将电极放到6mol?L-1NaOH溶液中,如图所示:
有甲和乙两位同学均想利用原电池反应来检测金属的活动性顺序,两人都使用镁片和铝片作电极,但甲同学将电极放到6mol?L-1 H2SO4溶液中,乙同学将电极放到6mol?L-1NaOH溶液中,如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com