
分析 每当雷电交加之际,可能发生如下反应:氮气与氧气在放电的条件下生成一氧化氮,一氧化氮被氧气氧化生成二氧化氮,二氧化氮与水反应生成硝酸和一氧化氮,由此分析解答.
解答 解:每当雷电交加之际,可能发生如下反应:氮气与氧气在放电的条件下生成一氧化氮,一氧化氮被氧气氧化生成二氧化氮,二氧化氮与水反应生成硝酸和一氧化氮,反应的化学方程式为:N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO,2NO+O2═2NO2,2NO2+H2O=2HNO3+NO,
故答案为:N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO;2NO+O2═2NO2;2NO2+H2O=2HNO3+NO.
点评 本题考查氮及其化合物的性质,一氧化氮极易被空气中的氧气氧化成二氧化氮,二氧化氮与水反应生成硝酸和一氧化氮,比较容易.


科目:高中化学 来源: 题型:选择题
| A. | ⑤③①④② | B. | ⑤③①②④ | C. | ②④①③⑤ | D. | ②④③①⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用惰性电极电解饱和食盐水时,阳极的电极反应式为2Cl--2e-=Cl2↑ | |
| B. | 二氧化碳通入碳酸钠溶液中CO2+CO32-+H+=2HCO3- | |
| C. | 粗铜精炼时,与电源正极相连的是纯铜,阳极反应式为Cu-2e-=Cu2+ | |
| D. | 钢铁发生电化学腐蚀的正极反应式:Fe-2e-=Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 表述1 | 表述2 | |
| A | 钠的金属性比铝强 | 钠原子核外电子数比铝少 |
| B | 金刚石的熔点高于晶体硅 | 原子半径Si大于C,键能Si-Si小于C-C |
| C | 离子晶体一般硬度较大,难压缩 | 离子晶体中阴、阳离子排列很有规律 |
| D | 相同条件下,分别完全燃烧等量的正丁烷和异丁烷,放出的热量相同 | 正丁烷与异丁烷互为同分异构体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为了减少脂肪的摄入,应该少吃肉制品,植物制品则可随意吃 | |
| B. | 保鲜膜、一次性食品袋的主要成分都是聚氯乙烯 | |
| C. | 蛋白质、淀粉和油脂都属于高分子化合物,一定条件下都能水解 | |
| D. | 鸡蛋白溶液中加入饱和硫酸铵溶液析出了沉淀,这种变化不是蛋白质的变性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
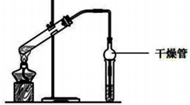 (1)乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业实验室用如图的装置制备乙酸乙酯.
(1)乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业实验室用如图的装置制备乙酸乙酯.| 物质 | 熔点/℃ | 沸点/℃ | 密度/(g/cm3) |
| 乙醇 | -144 | 78 | 0.789 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸 | -- | 338 | 1.84 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用铜做电极电解CuSO4溶液:2Cu2++2H2O═2Cu+O2↑+4H+ | |
| B. | 用银氨溶液检验乙醛的醛基:CH3CHO+2[Ag(NH3)2]++2OH-$\stackrel{水浴加热}{→}$CH3COO-+NH4++3NH3+2Ag↓+H2O | |
| C. | 苯酚钠溶液中通入少量CO2:2C6H5O-+H2O+CO2→2C6H5OH+CO32- | |
| D. | Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+═SO42-+3S↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 |  |  |  |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com