
【题目】“盐水动力”玩具车的电池以镁片、活性炭为电极,向极板上滴加食盐水后电池便可工作,电池反应为2Mg+O2 +2H2O=2Mg(OH)2。下列关于该电池的说法错误的是
A. 活性炭作为正极 B. 食盐水作为电解质溶液
C. 电池工作时镁片逐渐被消耗 D. 实现了电能向化学能的转化
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,Y和Z位于同一主族。m、n、P均为由这些元素组成的二元化合物,甲、乙、丙为其中三种元素对应的单质,丙为淡黄色固体, 易溶于XZ2,n是一种二元弱酸。上述物质的转化关系如图所示(反应条件省略)。下列说法正确的是

A. 原子半径:W B. W与X组成的化合物中只含有极性键
C. 简单氢化物的沸点:Y D. 非金属性:Y>Z>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A. 氯气与水反应:Cl2+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
B. 氯气与氢氧化钠溶液反应:Cl2+2OH-![]() Cl-+ClO-+H2O
Cl-+ClO-+H2O
C. 浓盐酸与二氧化锰共热:MnO2+4HCl(浓)![]() Mn2++2Cl-+Cl2↑+2H2O
Mn2++2Cl-+Cl2↑+2H2O
D. 漂白粉溶液中通入少量二氧化碳气体:Ca2++2ClO-+H2O+CO2![]() CaCO3↓+2H++2ClO-
CaCO3↓+2H++2ClO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是
A. 某温度Ksp(Ag2S)=6![]() 10-50(mol·L-1)3,Ksp(AgCl)=2
10-50(mol·L-1)3,Ksp(AgCl)=2![]() 10-6(mol·L-1)2,则2AgCl(g)+S2-(aq)
10-6(mol·L-1)2,则2AgCl(g)+S2-(aq) ![]() Ag2S(s)+2Cl-(aq)的平衡常数约为6.7
Ag2S(s)+2Cl-(aq)的平衡常数约为6.7![]() 1037mol·L-1
1037mol·L-1
B. pH相同的①CH3COONa ②NaHCO3 ③NaClO三种溶液中c(Na+):③<②<①
C. pH=a的氨水溶液,稀释10倍后,其pH=b,则b<a-1
D. 一定浓度的NaHS溶液在:c(Na+)+c(OH-)=c(H+)+c(HS-)+2c(H2S)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应表达正确的是( )
A. 1-丙醇与浓氢溴酸反应: CH3CH2 CH2OH + HBr ![]() CH3CH2 CH2Br + H2O
CH3CH2 CH2Br + H2O
B. 服用阿司匹林过量出现水杨酸(![]() )中毒反应, 可静脉注射 NaHCO3溶液:
)中毒反应, 可静脉注射 NaHCO3溶液:
![]() + 2 HCO3-→
+ 2 HCO3-→![]() + 2 CO2↑ + 2 H2O
+ 2 CO2↑ + 2 H2O
C. 向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH-![]() CH2BrCOO-+H2O
CH2BrCOO-+H2O
D. 向丙氨酸钠中加入足量盐酸:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题:
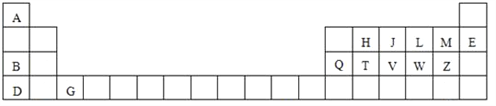
(1)原子半径最大的元素是_______;在化合物中只有负价的元素是 _______;属于副族元素是_______;适合作半导体材料的是_______,(只用表中的字母填写)
(2)V在周期表中的位置第_______周期第_______族。.
(3)M原子基态电子排布式为___________________________________。
L原子基态电子排布图为____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生对Na2S03与AgN03在不同pH下的反应进行探究
(1)测得Na2S03溶液pH=10,AgNO3溶液pH=5,二者发生水解的离子分别是__________;
(2)调节pH,实验记录如下:
实验 | pH | 现象 |
a | 10 | 产生白色沉淀,稍后溶解,溶液澄清 |
b | 6 | 产生白色沉淀,一段时间后,沉淀未溶 |
c | 2 | 产生大量白色沉淀,一段时间后,产生海绵状棕黑色物质X |
查阅资料得知:
①Ag2SO3:白色,难溶于水,溶于过量的Na2SO3溶液
②Ag2O棕黑色,不溶于水,能和酸反应,它和盐酸反应的化学方程式为 。
(3)该同学推测a中白色沉淀为Ag2SO4,依据是空气中的氧气可能参与反应,则生成硫酸银沉淀的离子方程式为 。
该同学设计实验确认了 a、b、c中的白色沉淀不是Ag2SO4,实验方法是:取b、c中白色沉淀, 置于Na2SO3溶液中,沉淀溶解。另取Ag2SO4固体置于足量 溶液中,未溶解。
(4)将c中X滤出、洗净,为确认其组成,实验如下:
I.向X中滴加稀盐酸,无明显变化
Ⅱ.向x中加人过量浓HNO3,产生红棕色气体。
Ⅲ.用 Ba(NO3)2 溶液、BaCl2溶液检验Ⅱ中反应后的溶液,前者无变化,后者产生白色沉淀.
①实验I的目的是 。
②根据实验现象,分析X是 。
③Ⅱ中反应的化学方程式是 。
(5)该同学综合以上实验,分析产生X的原因,认为随着酸性的增强,+4价硫的还原性增强,能被+1价银氧化。通过进一步实验确认了这种可能性,实验如下:

①通人Y后,瓶中白色沉淀转化为棕黑色,气体Y是 。
②白色沉淀转化为X的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对化工生产认识正确的是
A.海水提溴:一般需要经过浓缩、氧化、提取三个步骤
B.合成氯化氢:通入 H2 的量略大于 Cl2,可以使平衡正移
C.合成氨:采用 500℃的高温,有利于增大反应正向进行的程度
D.氯碱法:使用的粗盐事先不需要经过除杂处理
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com