
心脏起搏器电源—锂碘电池的电池反应为:2 Li(s) + I2 (s) = 2 LiI(s) ΔH
已知:4 Li(s) + O2 (g) = 2 Li2O(s) ΔH1
4 LiI(s) + O2 (g) = 2 I2 (s) + 2 Li2O(s) ΔH2 则下列说法正确的是( )
A.ΔH=1/2ΔH1 - ΔH2 B.ΔH=1/2ΔH1 + ΔH2
C.ΔH=1/2ΔH1 - 1/2ΔH2 D.ΔH=1/2ΔH1 +1/2ΔH2
科目:高中化学 来源:2013届浙江省东阳市黎明补校高三12月月考化学试卷(带解析) 题型:填空题
(共12分)碘在科研与生活中有重要应用。某兴趣小组用0.50mol·L-1KI、0.2%淀粉溶液、0.20mol·L-1K2S2O8、0.10mol·L-1Na2S2O3等试剂,探究反应条件对化学反应速率的影响。
已知:S2O82-+2I-==2SO42- +I2(慢) I2+2 S2O32-==2I-+S4O62-(快)
(1)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的__________耗尽后,溶液颜色将由无色变成为蓝色。为确保能观察到蓝色,S2O32-与S2O82-初始的物质的量需满足的关系为:n(S2O32-):n(S2O82-)_______。
(2)为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表:
表中Vx=_______________mL,理由是___________________。
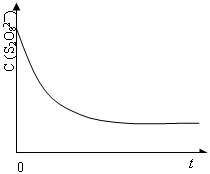
(3)已知某条件下,浓度c(S2O82-)~反应时间t的变化曲线如图13,若保持其他条件不变,请在答题卡坐标图中,分别画出降低反应温度和加入催化剂时c(S2O82-)~t的变化曲线示意图(进行相应地标注)
(4)碘也可用作心脏起搏器电源—锂碘电池的材料。该电池反应为:
2Li(s)+I2(s)=2LiI(s) △H
已知:4Li(s)+O2(g)=2Li2O(s) △H1
4LiI(s)+O2(g)=2I2(s)+2Li2O(s) △H2
则电池反应的△H=_______________。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河北省石家庄市第一中学高一下学期期中考试化学试卷(带解析) 题型:实验题
碘在科研与生活中有重要作用,某兴趣小组用0.50 mol·L—1KI、0.2%淀粉溶液、0.20 mol·L—1K2S2O8、0.10 mol·L—1Na2S2O3等试剂,探究反应条件对化学反应速率的影响。已知:S2O82—+ 2I— =" 2" SO42— + I2(慢) I2 + 2 S2O32— = 2I— + S4O62—(快(1)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的 耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色,S2O32—与S2O82—初始的物质的量需满足的关系为:n(S2O32—):n(S2O82—) 。
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
| 实验 序号 | 体积V/ml | ||||
| K2S2O8溶液 | 水 | KI溶液 | Na2S2O3溶液 | 淀粉溶液 | |
| ① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
| ② | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
| ③ | 8.0 | Vx | 4.0 | 4.0 | 2.0 |
查看答案和解析>>
科目:高中化学 来源:2015届河北省石家庄市高一下学期期中考试化学试卷(解析版) 题型:实验题
碘在科研与生活中有重要作用,某兴趣小组用0.50 mol·L—1KI、0.2%淀粉溶液、0.20 mol·L—1K2S2O8、0.10 mol·L—1Na2S2O3等试剂,探究反应条件对化学反应速率的影响。已知:S2O82—+ 2I— =" 2" SO42— + I2(慢) I2 + 2 S2O32— = 2I— + S4O62—(快(1)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的 耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色,S2O32—与S2O82—初始的物质的量需满足的关系为:n(S2O32—):n(S2O82—) 。
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
|
实验 序号 |
体积V/ml |
||||
|
K2S2O8溶液 |
水 |
KI溶液 |
Na2S2O3溶液 |
淀粉溶液 |
|
|
① |
10.0 |
0.0 |
4.0 |
4.0 |
2.0 |
|
② |
9.0 |
1.0 |
4.0 |
4.0 |
2.0 |
|
③ |
8.0 |
Vx |
4.0 |
4.0 |
2.0 |
表中Vx = ml,理由是 。
(3)已知某条件下,浓度c(S2O82—)随反应时间t的变化曲线如图,若保持其它条件不变,请在答题卡坐标图中,分别画出降低反应温度和加入催化剂时c(S2O82—)随反应时间t的变化曲线示意图(进行相应的标注)。
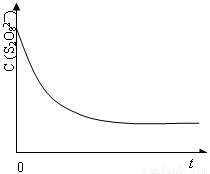
(4)碘也可用作心脏起搏器电源—锂碘电池的材料,
该电池反应为:2 Li(s) + I2 (s) =" 2" LiI(s) ΔH
已知:4 Li(s) + O2 (g) =" 2" Li2O(s) ΔH1
4 LiI(s) + O2 (g) =" 2" I2 (s) + 2 Li2O(s) ΔH2
则电池反应的ΔH = ;还原剂是 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年浙江省东阳市黎明补校高三12月月考化学试卷(解析版) 题型:填空题
(共12分)碘在科研与生活中有重要应用。某兴趣小组用0.50mol·L-1KI、0.2%淀粉溶液、0.20mol·L-1K2S2O8、0.10mol·L-1Na2S2O3等试剂,探究反应条件对化学反应速率的影响。
已知:S2O82-+2I-==2SO42- +I2(慢) I2+2 S2O32-==2I- +S4O62- (快)
(1)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的__________耗尽后,溶液颜色将由无色变成为蓝色。为确保能观察到蓝色,S2O32-与S2O82-初始的物质的量需满足的关系为:n(S2O32-):n(S2O82-)_______。

(2)为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表:
表中Vx=_______________mL,理由是___________________。
(3)已知某条件下,浓度c(S2O82-)~反应时间t的变化曲线如图13,若保持其他条件不变,请在答题卡坐标图中,分别画出降低反应温度和加入催化剂时c(S2O82-)~t的变化曲线示意图(进行相应地标注)

(4)碘也可用作心脏起搏器电源—锂碘电池的材料。该电池反应为:
2Li(s)+I2(s)=2LiI(s) △H
已知:4Li(s)+O2(g)=2Li2O(s) △H1
4LiI(s)+O2(g)=2I2(s)+2Li2O(s) △H2
则电池反应的△H=_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com