
【题目】等电子体的结构相似、物理性质相近,称为等电子原理。如N2和CO为等电子体。下表为部分元素等电子体分类、空间构型表。
等电子体类型 | 代表物质 | 空间构型 |
四原子24电子等电子体 | SO3 | 平面三角形 |
四原子26电子等电子体 | SO32- | 三角锥形 |
五原子32电子等电子体 | CCl4 | 四面体形 |
六原子40电子等电子体 | PCl5 | 三角双锥形 |
七原子48电子等电子体 | SF6 | 八面体形 |
由第一、二周期元素组成,与F2互为等电子体的离子有__________。
 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
【题目】标准状况下VL氨气溶解在1L水中,所得溶液的密度为ρ g/ml,质量分数为ω,物质浓度为c mol/L,则下列关系中正确的是( )
A.c= ![]()
B.ω= ![]()
C.ω= ![]()
D.ρ= ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】霾是空气中的灰尘、硫酸、硝酸等颗粒物组成的气溶胶系统造成的视觉障碍,属于大气污染。如图为霾的主要成分示意图,下列说法不正确的是

A. 用丁达尔现象可以鉴别SO2和SO3的混合气体和有霾的空气
B. “光化学烟雾”“硝酸型酸雨”的形成与氮氧化合物有关
C. 苯、甲苯、二甲苯都属于芳香烃
D. SO2和NxOy都属于酸性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图装置进行实验,并回答下列问题。
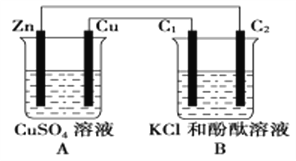
(1)判断装置的名称:A池为________,B池为________。
(2)锌极为________极,电极反应式为___________________________________。
铜极为________极,电极反应式为___________________________________。
石墨棒C1为________极,电极反应式为_________________________________。
石墨棒C2附近发生的实验现象为_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国政府为了消除碘缺乏病,在食盐中均加入一定量的“碘”。下列关于“碘盐”的说法中错误的是
A. “碘盐”就是NaI
B. “碘盐”就是适量的碘酸钾(KIO3)与食盐的混合物
C. “碘盐”应保存在阴凉处
D. 使用“碘盐”时,切忌高温煎炒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. 从CH4、NH4+、SO42-为正四面体结构,可推测PH4+、PO43-也为正四面体结构
B. 不同非金属元素原子之间形成的化学键都是极性键
C. 水的沸点比硫化氢的高,是因为H2O分子间存在氢键,H2S分子间不能形成氢键
D. 某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.分子式相同,各元素质量分数也相同的物质是同种物质
B.通式相同的不同物质一定属于同系物
C.分子式相同的不同物质一定是同分异构体
D.相对分子质量相同的不同物质一定是同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据方程式KClO3+6HCl=KCl+3Cl2↑+2H2O 回答下列问题
(1)氧化剂与还原剂的物质的量之比是:
(2)盐酸体现出的性质有:
(3)用双线桥表示出电子转移的方向和数目:KClO3+6HCl=KCl+3Cl2↑+2H2O
(4)当被氧化的HCl为73克时,转移的电子的数目为(填具体数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气是一种重要化合物,在工农业生产、生活中有着重要作用。
(1)“氨的催化氧化”是工业生产硝酸的重要步骤。某化学课外活动小组设计了如下装置模拟该实验过程,并用水吸收制取硝酸(固定装置略去):
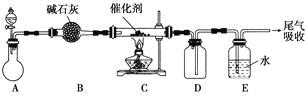
①A装置的分液漏斗中盛放浓氨水,则烧瓶中盛放的药品应该是________。
②C装置中发生反应的化学方程式为________________。
③反应后,装置E中除存在较多的H+外,还可能存在的一种离子是________,试设计实验证明这种离子的存在_____________________。
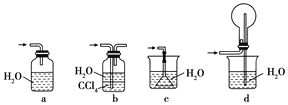
④下列哪些装置可以同时起到装置D和E的作用________(填代号)。
(2)若将氯气和氨气在集气瓶中混合,会出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,请写出反应的化学方程式:________________(不必配平),该反应生成的还原产物的化学键类型是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com