
| 1 |
| 2 |


 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源: 题型:
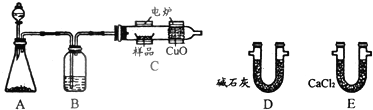
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X、Y、Z的浓度相等 |
| B、X、Y、Z的分子数比为1:3:2 |
| C、Z的生成速率是X的生成速率的二倍 |
| D、单位时间内生成n mol X,同时生成3n mol Y |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、生铁、不锈钢和黄金都属于合金 |
| B、水泥、玻璃、陶瓷均属于无机非金属材料 |
| C、淀粉、油脂、蛋白质都属于天然高分子化合物 |
| D、天然气、石油液化气和汽油的主要成分都属于烃类 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu2+、NH4+、SO42-、OH- |
| B、Ag+、NO3-、Cl-、K+ |
| C、H+、Al3+、NO3-、Cl- |
| D、H+、Na+、NO3-、Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NO3-、Al3+、K+ |
| B、SiO32-、AlO2-、K+ |
| C、SO42-、Cu2+、Na+ |
| D、Ba2+、Na+ NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将pH=4的某酸稀释10倍,测得其pH<5,则该酸为弱酸 |
| B、相同pH的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(Na2CO3)<c(CH3COONa) |
| C、0.1 mol/L的NaHA溶液pH=5,则溶液:c(HA-)>c(H+)>c(A2-)>c(H2A) |
| D、向NH4HSO4溶液中滴加NaOH溶液至中性,所得混合液:c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将化学能转化为电能电池 |
| B、放电时,H+向正极移动 |
| C、正极反应式为:O2+2H2O+4e-═4OH- |
| D、负极反应式可能为:S2-+4H2O-8e-═SO42-+8H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com