
在短周期中X、Y可形成化合物XY3,下列叙述错误的是( )
A. 若Y的原子序数为m ,则X的原子序数可能为m+4
B. XY3可能是离子化合物
C. X、Y可能同周期,也可能同主族
D. XY3可能是原子晶体
科目:高中化学 来源:2016-2017学年河南省高一上8月摸底化学试卷(解析版) 题型:选择题
鉴别物质的方法错误的是( )
A.用酚酞鉴别食盐水和稀醋酸
B.用水鉴别生石灰和石灰石
C.用燃着的木条鉴别空气和二氧化碳
D.用氯化钡溶液鉴别稀盐酸和稀硫酸
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上开学测化学试卷(解析版) 题型:选择题
我国的纳米基础研究能力已跻身于世界前列,曾制得一种合成纳米材料,其化学式为RN。已知该化合物中的Rn+核外有28个电子,则R元素位于元素周期表的( )
A. 第三周期第ⅤA族 B. 第四周期第ⅤA族
C. 第五周期第ⅢA族 D. 第四周期第ⅢA族
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上开学测化学试卷(解析版) 题型:推断题
X、Y、Z、W四种短周期元素在周期表中的位置关系如图:若Y元素原子的最外层电子数是电子层数的3倍。
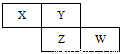
(1) W的原子结构示意图为_____________。
(2)一定条件下,X的最低价氢化物与X的某种氧化物按2:3物质的量比混合恰好反应生成X单质和水,该氧化物的化学式为____________。
(3)写出铜片置于Z的最高价氧化物水化物稀溶液,没有明显变化。加热,依然如故。再通入空气,溶液就逐渐变蓝,反应的离子方程式:____________。
II.若Y和Z的核外电子数之和为20 。
(4)相对分子质量为28 的Y的氢化物电子式为____________
(5)W的一种单质溶于足量浓硝酸,反应过程转移电子物质的量是该单质的20倍。反应的化学方程式:____________。
(6)X单质熔点2076℃。沸点3927℃ ,晶体硬度近似于金刚石,则X单质晶体属于_______晶体;Z单质晶体结构与金刚石类似,晶体内化学键键角为____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上开学测化学试卷(解析版) 题型:选择题
化学反应可视为旧键断裂和新键形成的过程。共价键的键能是两种原子间形成共价键(或其逆过程)时释放(或吸收)的能量。己知H-H键能为43kJ/mol , H-N键能为391kJ/mol,根据化学方程式:N2(g)+3H2(g)=2NH3(g)△H=-92.4 kJ/mol,则N≡N键的键能是( )
A.431kJ/mol B.946 kJ/mol C.649 kJ/mol D.869 kJ/mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上开学测化学试卷(解析版) 题型:选择题
下列推断合理的是( )
A.Cu的活动性排在H之后,不能与浓H2SO4发生反应
B.金刚石是自然界中硬度最大的物质,不能与氧气发生反应
C.明矾[KAl(SO4)2·12H2O]在水中能形成Al(OH)3胶体,可用作净水剂
D.将SO2通入品红溶液,溶液褪色后加热恢复原色:将SO2通入溴水,溴水褪色后加热也能恢复原色
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上开学测化学试卷(解析版) 题型:填空题
甲醇是一种重要的化工原料,又是一种可再生资源,具有开发和应用的广阔前景。
(1)已知:CH3OH(g)=HCHO(g)+H2(g) △H=+84kJ/mol
2H2(g)+O2(g)=2H2O(g) △H=-484kJ/mol
①工业上常以甲醇为原料制取甲醛,请写出CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式:________________。
②在上述制备甲醛时,常向反应器中通入适当过量的氧气,其目的是_________________。
(2)工业上可用如下方法合成甲醛,化学方程式为CO(g)+2H2(g)=CH3OH(g),已知某些化学键的键能数据如下表:
化学键 | C-C | C-H | H-H | C-O | C=O | O-H |
键能/kJ/mol | 348 | 413 | 436 | 358 | x | 463 |
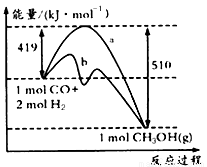
请回答下列问题:
①如图中曲线a到曲线b的措施是_______________。
②已知CO中的C与O之间为三键,其键能为xkJ/mol,则x=___________。
(3)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。
①该电池正极的电极反应式为____________________。
②若以该电池为电源,用石墨作电极电解200mL含有如下离子的溶液。
离子 | Cu2+ | H+ | Cl- | SO42- |
c/mol/L | 0.5 | 2 | 2 | 0.5 |
电解一段时间后,当两极收集到相同体积(相同条件下)的气体时(忽略溶液体积的变化及电极产物可能存在的溶液现象)阳极上收集到氧气的质量为_____________。
(4)电解水蒸气和CO2产生合成气(H2+CO),较高温度下(700-1000℃),在SOEC两侧电极上施加一定的直流电压,H2O和CO2在氢电极发生还原反应产生O2-,O2-穿过致密的固体氧化物电解质层到达氧电极,在氧电极发生氧化反应得到纯O2。由右图可知A为直流电源的 (填“正极”或“负极”),请写出以H2O为原料生成H2的电极反应式:____________。

查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上开学测化学试卷(解析版) 题型:选择题
在一定温度下.10mL0.40mol/LH2O2发生催化分解.不同时刻测定生成O2的休积(己折算为标准状况)如下表。

下列叙述不正确的是(溶液体积变化忽略不计)( )
A.0~6min的平均反应速率:v(H2O2)≈3.3×10-2mol/(L•min)
B.6~10min的平均反应速率:v(H2O2)<3.3×10-2mol/(L•min)
C.反应至6min时,c(H2O2) = 0.30mol/L
D.反应至6min时,H2O2分解了50%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com