
【题目】下列各物质中酸性最弱的是
A. H2SiO3 B. HClO4 C. H2SO4 D. H2CO3
科目:高中化学 来源: 题型:
【题目】在氯化氢分子中,形成共价键的原子轨道是( )
A.氯原子的2p轨道和氢原子的1s轨道
B.氯原子的2p轨道和氢原子的2p轨道
C.氯原子的3p轨道和氢原子的1s轨道
D.氯原子的2p轨道和氢原子的3p轨道
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应A(g)+2B(g)===3C(g)+4D(g)中,表示该反应速率最快的是
A. v(A)=0.2 mol/(L·s) B. v(B)=0.6 mol/(L·s)
C. v(C)=0.8 mol/(L·s) D. v(D)=1 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知用硫酸酸化的草酸(H2C2O4)溶液能与KMnO4溶液反应.某化学小组研究发现,少量MnSO4可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
(1)常温下,探究不同的初始pH和草酸溶液浓度对反应速率的影响,设计如下实验,则A=_____,C=_____,E=_____。
实验编号 | 温度 | 初始pH | 0.1mol/L草酸溶液体积/mL | 0.01mol/LKMnO4 溶液体积/mL | 蒸馏水体积/mL | 待测数据(混合液褪色时间/s) |
① | 常温 | 1 | 20 | 50 | 30 | t1 |
② | 常温 | A | B | C | 30 | t2 |
③ | 常温 | 2 | 40 | D | E | t3 |
(2)该反应的离子方程式__________________________________________________。
(3)若t1<t2,则根据实验①和②得到的结论是_____________。
(4)小组同学发现每组实验反应速率随时间的变化总是如图,
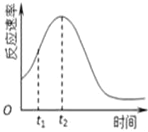
其中t1~t2时间内速率变快的主要原因可能是:
①__________________________________________;
②___________________________________________。
(5)化学小组用滴定法测定KMnO4溶液物质的量浓度:取ag草酸晶体(H2C2O4·2H2O,摩尔质量126g/mol)溶于水配成250mL溶液,取25.00mL溶液置于锥形瓶中,加入适量稀H2SO4酸化,再用KMnO4溶液滴定至终点,重复滴定三次,平均消耗KMnO4溶液VmL。该KMnO4溶液的物质的量浓度为_____mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表。
元索 | 相关信息 |
T | T元素可形成自然界硬度最大的单质 |
W | W与T同周期,核外有一个未成对电子 |
X | X原子的第一离能至第四电离能分别I1=578 kJ/mol; I2= l817 kJ/mol; I3=2745 kJ/mol;I4=11575kJ/mol |
Y | 常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质 |
Z | Z的一种同位素的质量数为63,中子数为34 |
(1)TY2的结构式是__________是__________(填“极性分子”或“非极性分子”),1mol该分子中存在________个σ键。

(2)基态Y原子中,电子占据的最高能层符号为__________,该能层具有的原子轨道数为_____________、电子数为_________。Y、氧、W元素的电负性由大到小的顺序为_________(用元素符号作答)。
(3)已知Z的晶胞结构如图所示,又知Z的密度为a g/cm3,则Z 的半径为___________pm;ZYO4常作电镀液,其中YO42-的等电子体是__________,其中Y原子的杂化轨道类型是___________。元素Z与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z +HCl+O2=ZC1+HO2,HO2(超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示正确的是___________。
A.O2是氧化剂 B.HO2是氧化产物
C.HO2在碱中能稳定存在 D.1 mol Z参加反应有1 mol电子发生转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A.两个原子间形成的共价键键能越大,键长越短,键越牢固
B.两个原子半径之和就是所形成的共价键键长
C.两个原子间键长越长,键越牢固
D.键的强度与键长无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质转化关系的说法中不正确的是( )

A. 图1中甲可能是Cl2,X可能是Fe
B. 图2中反应一定是置换反应或复分解反应
C. 图3中是向某溶液中滴加NaOH溶液的变化图像,原溶质可能是Al2(SO4)3
D. 图4中a可能为NaOH,b可能为Na2CO3,c可能为NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下0.1mol/L CH3COOH溶液中c(H+)=1.32×10-3mol/L,则该CH3COOH溶液中的水的离子积常数Kw是
A.1×10-14B.1×10-13C.1.32×10-14D.1.32×10-15
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com