
| 元素 | A | B | C | D |
| 性质或 结构信息 |
其单质和化合物的焰色均为黄色 | 其氢化物的水溶液能腐蚀玻璃 | 其单质在空气中体积含量最多 | 地壳中含量最多的金属元素 |
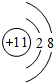
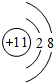
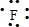
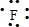
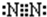
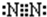
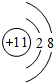 ,F原子电子式为
,F原子电子式为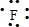 ,N2的电子式为
,N2的电子式为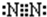 ,
,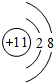 ;
;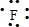 ;
;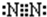 ;
; 

科目:高中化学 来源: 题型:
| 元素 | A | B | C | D | E |
| 有关性质或结构信息 | 单质是空气中主要成分之一,其氢化物水溶液呈碱性 | 原子核外有两个未成对电子 | 日常生活中常见的金属,通常用电解法冶炼其单质 | 其简单阴离子带两个单位负电荷 | 单质有毒,常温下为有色气体,常用于自来水消毒 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | A | B | C | D |
| 性质 或 结构 信息 |
其单质和化合物的焰色均为黄色 | 其氢化物的水溶液能腐蚀玻璃 | 湿润的红色石蕊试纸遇其最低价氢化物变蓝 | 其原子核外有13种运动状态的电子 |


| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2011-2012学年上海市宝山区吴淞中学高一(上)期末化学试卷(解析版) 题型:填空题
| 元素 | A | B | C | D |
| 性质或 结构信息 | 其单质和化合物的焰色均为黄色 | 其氢化物的水溶液能腐蚀玻璃 | 其单质在空气中体积含量最多 | 地壳中含量最多的金属元素 |
查看答案和解析>>
科目:高中化学 来源:2009年上海市黄浦区高考化学二模试卷(解析版) 题型:解答题
| 元素 | A | B | C | D |
| 性质 或 结构 信息 | 其单质和化合物的焰色均为黄色 | 其氢化物的水溶液能腐蚀玻璃 | 湿润的红色石蕊试纸遇其最低价氢化物变蓝 | 其原子核外有13种运动状态的电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com