
100mLij��Һ�п��ܺ���H+��NH4+��Mg2+��Al3+��Fe3+��CO32����SO42����NO3���еļ��֣���������п���������H2����������NaOH��Һ��������ɫ�������Ҳ����ij����������NaOH�����ʵ���֮��Ĺ�ϵ��ͼ��ʾ��

��1����Һ��һ�����е��������� ��һ�������е������� ��
��2��C��D�����ӷ���ʽΪ ��
��3����A��B��C��D���й����ݿɼ������ij�������ӵ����ʵ���Ũ�ȷֱ�Ϊ mol•L��1�� mol•L��1

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ�߶���ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���з���ʽ��д��ȷ����
A��̼��ĵ��뷽��ʽ��H2CO3  2H+ + CO32��
2H+ + CO32��
B. ����ˮ��: S2-+2H2O H2S +2OH-
H2S +2OH-
C����AgI����Һ�еμ�Na2S������Һ��2Ag+ (aq)+ S2��(aq) = Ag2S(s)
D���ô����ˮ���� 2CH3COOH + CaCO3 = 2CH3COO- + Ca2+ + H2O + CO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ�߶���11���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ʵı仯������ͨ��һ����ѧ��Ӧ��ɵ���
A��NO2��HNO3 B��Cl2��HClO C��SiO2��H2SiO3 D��H2SO4(Ũ����SO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���Ĵ�ʡ��һ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A��Ħ�����߸�����������֮һ
B�����1 molij��������Ϊ22.4L����ⶨ����һ���DZ�״��
C������һ�����ʵ���Ũ�ȵ�NaCl��Һʱ�����ݡ���ҡ�Ⱥ���Һ����ڿ̶��ߣ��ټ�ˮ���̶���
D������ֻ�ܵ����H�������������������ӵĻ����ﶼ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ��ˮ�и�����ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪NH4 CuSO3��������10 mol��L������Һ����ȣ��������������к�ɫ�������� �ڲ����̼�����ζ���������Һ������ɫ���ݴ��ж�����˵����ȷ����
A����Ӧ�������������� B��NH4 CuSO3����Ԫ�ر�����
C���̼�����ζ�������ǰ��� D��1 mol NH4 CuSO3��ȫ��Ӧת��0.5 mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������ʡ������ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ������
A��B��C��D��E��F��Ԫ�����ڱ�ǰ�������еij���Ԫ�أ�ԭ�������������������Ϣ���±���
Ԫ�� | �����Ϣ |
A | ���γ���Ȼ��Ӳ�����ĵ��� |
B | ��AԪ��ͬ���ڣ�����������δ�ɶԵ��� |
C | ����������������Ӳ�����3�� |
D | ��һ�����������ĵ����ֱܷ���I1=578KJ/mol��I2=1817KJ/mol��I3=2745KJ/mol, I4=11575KJ/mol |
E | ���³�ѹ�£�E�ĵ����ǹ��壬�����������γ��������Ҫ���� |
F | F��һ��ͬλ�ص�������Ϊ63��������Ϊ34 |
��1��A��B��CԪ�صĵ�һ�������ɴ�С��˳��Ϊ ����Ԫ�ط��ű�ʾ����F�Ļ�̬ԭ�Ӻ�������Ų�ʽΪ ��
��2��AE2��һ�ֳ��õ��ܼ����� ������ԡ��Ǽ��ԡ������ӣ������ЦҼ���м�������Ϊ ��
��3��д��D��NaOH��Һ��Ӧ���� �ӷ���ʽ ��DB�γɵľ�������ʯ���ƣ������� ���塣B������⻯������Һ����������
�ӷ���ʽ ��DB�γɵľ�������ʯ���ƣ������� ���塣B������⻯������Һ����������


��4����֪F�ľ���ṹ��ͼ��ʾ����֪F���ܶ�Ϊ9��00g��cm-3�����߳�Ϊ ��FEC4�������Һ������EC42-�Ŀռ乹���� ������Eԭ�ӵ��ӻ���������� ��
��5��F��һ���Ȼ��ᄃ����ṹ��ͼ��ʾ�����Ȼ���Ļ�ѧʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭ʡ�����и�����ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪H2S+I2=2HI+S��������S2����Fe2+��Br����I����0.1mol����Һ��ͨ��Cl2��ͨ��Cl2���������״��������Һ��������ӵ����ʵ�����ϵͼ��ȷ����
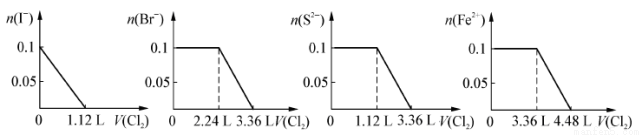
A B C D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���㽭ʡ̨���и�һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���г�ȥ���ʵķ�����ȷ����
A����ȥN2�е�����O2��ͨ�����ȵ�CuO��ĩ
B����ȥCO2�е�����HCl��ͨ��Na2CO3��Һ
C����ȥKCl��Һ�е�����K2CO3����������������
D����ȥKCl��Һ�е�����MgCl2����������NaOH��Һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��㶫ʡ��ݸ����У������ѧ���������ۻ�ѧ�Ծ��������棩 ���ͣ������
��A��B��C��D��E���ֶ�����Ԫ�أ���֪���ڵ�A��B��C��D����Ԫ��ԭ�Ӻ����56�����ӣ������ڱ��е�λ����ͼ��ʾ��E�ĵ��ʿ����ᷴӦ��1molE���������������ã��ڱ�״�����ܲ���33.6LH2��E����������A�������Ӻ�����Ӳ�ṹ��ȫ��ͬ��

�ش��������⣺
��1��A��E�γɵĻ�����Ļ�ѧʽ�� ��
��2��B����������ﻯѧʽΪ ��C��Ԫ������Ϊ ��
D�ĵ�����ˮ��Ӧ�ķ���ʽΪ_ ��
��3����D��E�γɵĻ������ˮ��Һ�е����ռ���Һֱ���������۲쵽�������� ���йط�Ӧ�����ӷ���ʽΪ �� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com