
【题目】(1)官能团与有机物的性质密切相关。
①下列物质易溶于水的是_____________________(填字母)。
a.异丁烷 b.乙醇 c.氯乙烯
②下列物质不能发生水解反应的是_____________________(填字母)。
a.葡萄糖 b.溴乙烷 c.乙酸乙酯
③可用酸性KMnO4溶液鉴别的一组物质是_____________________(填字母)。
a.甲烷与乙烷 b.乙烯与乙炔 c.苯和甲苯
(2)对香豆酸的结构简式如右图所示。
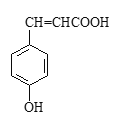
①对香豆酸分子中位于同一平面的碳原子最多有_____________________个。
②1mol对香豆酸最多可与____________________ molH2发生加成反应。
③聚对香豆酸的结构简式为____________________。
(3)D(胡椒醛)是一种食品香料,以A为原料制备D的一种合成路线如下:
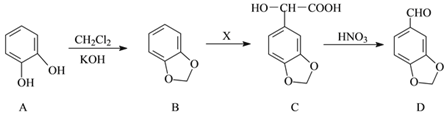
①A→B的反应类型是____________________;C中的含氧官能团名称为_____________________和____________________(填二种)。
②X的分子式为C2H2O3,B→C为加成反应,X的结构简式为____________________。
③芳香化合物Y是D的同分异构体,Y既能与NaHCO3反应生成CO2又能发生银镜反应,苯环上的一硝基取代物只有二种。符合题意的Y的结构简式为____________________。
【答案】 b a c 9 4 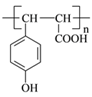 取代反应 醚键 羟基和羧基
取代反应 醚键 羟基和羧基 ![]()
![]()
【解析】(1)①a.异丁烷难溶于水,a错误;b.乙醇与水互溶,b正确;c.氯乙烯难溶于水,c错误;答案选b;②a.葡萄糖的单糖,不能发生水解反应,a正确;b.溴乙烷是卤代烃,能发生水解反应,b错误;c.乙酸乙酯属于酯类,能发生水解反应,c错误,答案选a;③a.甲烷与乙烷都不能使酸性高锰酸钾溶液褪色,不能鉴别甲烷与乙烷,a错误;b.乙烯与乙炔都能使酸性高锰酸钾溶液褪色,不能鉴别,b错误;c.甲苯能使酸性高锰酸钾溶液褪色,能鉴别苯和甲苯,c正确,答案选c;(2)①由于碳碳双键、碳氧双键和苯环均是平面形结构,所以对香豆酸分子中位于同一平面的碳原子最多有9个。②碳碳双键和苯环均与氢气发生加成反应,1mol对香豆酸最多可与4molH2发生加成反应。③碳碳双键发生加聚反应生成聚对香豆酸,其结构简式为 。(3)①A→B是酚羟基发生分子内脱水,反应类型是取代反应;C中的含氧官能团名称为醚键、羟基和羧基。②X的分子式为C2H2O3,B→C为加成反应,因此根据C的结构简式可知X的结构简式为OHC-COOH。③芳香化合物Y是D的同分异构体,Y既能与NaHCO3反应生成CO2又能发生银镜反应,含有羧基与醛基,苯环上的一硝基取代物只有二种,说明苯环上含有取代基且是对位的,则符合题意的Y的结构简式为
。(3)①A→B是酚羟基发生分子内脱水,反应类型是取代反应;C中的含氧官能团名称为醚键、羟基和羧基。②X的分子式为C2H2O3,B→C为加成反应,因此根据C的结构简式可知X的结构简式为OHC-COOH。③芳香化合物Y是D的同分异构体,Y既能与NaHCO3反应生成CO2又能发生银镜反应,含有羧基与醛基,苯环上的一硝基取代物只有二种,说明苯环上含有取代基且是对位的,则符合题意的Y的结构简式为![]() 。
。


 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
【题目】25℃时,向20mL0.1mol/LHAuCl4溶液中滴加0.1mol/LNaOH溶液,滴定曲线如图1,含氯微粒的物质的量分数(δ)随pH变化关系如图2,则下列说法不正确的是
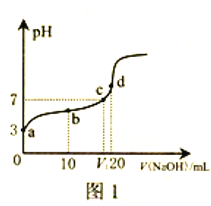
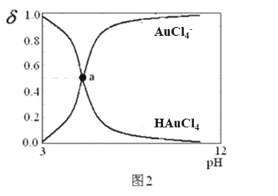
A. 在c点溶液中:c(Na+)=c(AuCl4-)
B. a点对应溶液pH约为5
C. 25℃时,HAuCl4的电离常数为1×10-3
D. d点时,溶液中离子浓度大小关系为:c(Na+)>c(AuCl4-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可降解聚合物P的合成路线如下:
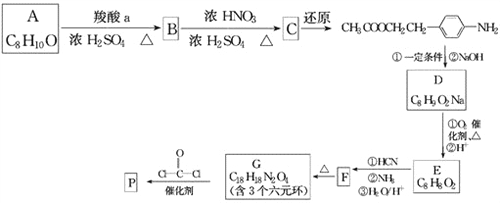
已知:
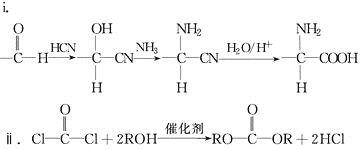
(R为烃基)
(1)A的含氧官能团名称是________。A的核磁共振氢谱共有_____组峰
(2)羧酸a的电离方程式是_______________________________________________。
(3)B→C的化学方程式是_________________________________________________。
(4)化合物D苯环上的一氯代物有_______________种。
(5)E→F中反应①和②的反应类型分别是_______________、_________________。
(6)F的结构简式是_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),
CO(g)+H2O(g),
其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K =__________________。
(2)该反应为__________反应(“吸热”或“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是_______________。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为________℃。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“民以食为天,食以安为先”,下列做法会危害食品安全的是
A. 回收餐桌废油加工成化工原料 B. 给蔬菜瓜果喷洒甲醛溶液
C. 做菜时加适量的酱油调味細味 D. 用食盐作食物防腐剂
查看答案和解析>>
科目:高中化学 来源: 题型:
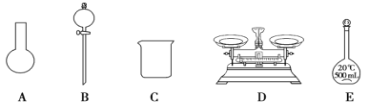
【题目】I.如图所示为常见玻璃仪器的部分结构:
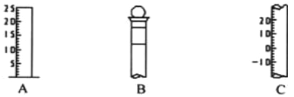
(1)请写出所列仪器的名称: A______,B_______,C_______;
(2)仪器 B 使用前必须__________________。
(3)仪器 B 上标记有______(填序号);①质量 ②温度 ③刻度线 ④浓度 ⑤容积
II.已知某“84 消毒液”瓶体部分标签如图所示,该“84 消毒液”通常稀释 100 倍(体积之比)后使用。请回答下列问题:
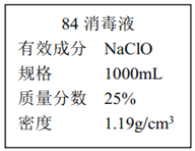
(1)该“84 消毒液”的物质的量浓度约为_______mol·L-1。(保留两位有效数字)
(2)某同学取100 mL该“84 消毒液”,稀释后用于消毒,稀释后的溶液中 c (Na+)=_____。
(3)该同学参阅该“84 消毒液”的配方,欲用 NaClO 固体配制 250 mL含 NaClO 质量分数为 25%的消毒液。下列说法不正确的是________(填序号)。
a.如图所示的仪器中,有三种是不需要的,还需要其它玻璃仪器
b.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
c.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
(4) “84 消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用 98%(密度为1.84g·cm-3)的浓硫酸配制2 L 2.3 mol·L-1 的稀硫酸用于增强“84 消毒液”的消毒能力。需用浓硫酸的体积为______ mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在空气中,有下列反应发生: ①N2 + O2 = 2NO;②2NO+O2=2NO2;③3NO2 + H2O = 2HNO3 + NO;④ 2SO2+O2 = 2SO3;⑤ SO3 + H2O = H2SO4; ⑥SO2+H2O![]() H2SO3; ⑦3O2 = 2O3,其中属于氧化还原反应的是( )
H2SO3; ⑦3O2 = 2O3,其中属于氧化还原反应的是( )
A. ①②③④ B. ①②③④⑦ C. ①②④⑦ D. ①②③④⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量浓度相同的三种酸HX、HY、HZ的溶液,其pH依次为4、5、6,则KX、KY、KZ的碱性由强到弱的顺序是( )
A. KX、KZ、KY B. KX、 KY、KZ
C. KZ、KY 、KX D. KY、KZ、KX
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备纯净的氯化锌时,将含杂质的氯化锌溶于过量盐酸中,为了除去杂质需调节溶液的pH到4,应加入的试剂是( )
A. ZnCl2 B. ZnO C. NaOH D. NH3·H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com