
阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是
A.2.24LCO2中含有的原子数为0.3×6.02×1023
B.0.1L3mol·L-1的NH4NO3溶液中含有的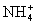 数目为0.3×6.02×1023
数目为0.3×6.02×1023
C.5.6g铁粉与硝酸反应失去的电子数一定为0.3 ×6.02×1023
D.4.5 SiO2晶体中含有的硅氧键数目为0.3 ×6.02×1023
科目:高中化学 来源: 题型:
下列反应,属于氧化还原反应,但水既不作氧化剂又不作还原剂的是( )
A.SO3 + H2O = H2SO4
B.2Na2O2 + 2H2O = 4NaOH + O2↑
C.2F2 + 2H2O = 4HF + O2 ↑
D.2Na + 2H2O = 2NaOH + H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.1.00mol NaCl中含有6.02×1023个NaCl分子
B. 1.00mol NaCl中,所有Na+的最外层电子总数为8×6.02×1023
C.欲配置1.00L ,1.00mol.L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中
D.电解58.5g 熔融的NaCl,能产生22.4L氯气(标准状况)、23.0g金属钠
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数,下列叙述正确的是( )
A.24 g镁的原子最外层电子数为NA
B.1 L 0.1 mol·L-1乙酸溶液中H+数为0.1NA
C.1 mol甲烷分子所含质子数为10NA
D.标准状况下,22.4 L乙醇的分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
NA代表阿伏加德罗常数,下列叙述错误的是
A.10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2SO4的质量分数为9.8%
B.在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移2NA个电子
C.标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g
D.一定温度下,1 L 0.50 mol·L-1 NH4Cl溶液与2 L 0.25 mol·L-1 NH4Cl溶液含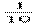 物质的量不同
物质的量不同
查看答案和解析>>
科目:高中化学 来源: 题型:
在三个密闭容器中分别充入Ne,H2,O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从大到小的顺序是
A.p(Ne)>p(H2)>p(O2) B.p(O2)> p(Ne)> p(H2)
C. p(H2)> p(O2)> p(Ne) D. p(H2)> p(Ne)> p(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
在体积相同的两个密闭器中分别充满O2、O3气体,当这两个容器内温度和气体密度相等时,下列说法正确的是
A.两种气体的压强相等
B.O2比O3的质量小
C.两种气体的分子数目相等
D.两种气体的氧原子数目相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com