
【题目】下图是铜锌原电池示意图。图2中,x轴表示实验时流入正极的电子的物质的量,y轴表示( )

A. c(H+) B. V(H2) C. m(溶液) D. m(Cu)
 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
【题目】高铁酸钾是一种新型、高效、多功能水处理剂,工业上采用向KOH溶液中通入氯气,然后再加入![]() 溶液的方法制备
溶液的方法制备![]() ,发生反应:
,发生反应:
①![]() (未配平);
(未配平);
②![]() 。
。
下列说法正确的是
A.若反应①中![]() ,则氧化剂与还原剂的物质的量之比为2:1
,则氧化剂与还原剂的物质的量之比为2:1
B.反应①中每消耗4 mol KOH,吸收标准状况下![]()
C.氧化性:![]()
D.若反应①的氧化产物只有KClO,则得到![]() 时消耗
时消耗![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A. 按系统命名法,化合物![]() 的名称为2-乙基丙烷
的名称为2-乙基丙烷
B. 丙烯分子中,最多有7个原子共面
C. 蔗糖和淀粉的水解产物相同且均为葡萄糖
D. 向鸡蛋清中加入Pb(CH3COO)2或(NH4)2SO4溶液均会产生沉淀,两者的原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将V 1 mL 0.1mol·L-1的Fe2(SO4)3溶液与2mL 0.1mol·L-1KI溶液混合,待充分反应后,下列方法可证明该反应具有一定限度的是( )
A.若V1<1,加入淀粉B.若V1≤1,加入KSCN溶液
C.若V1≥1,加入AgNO3溶液D.加入Ba(NO3)2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成聚丙烯腈纤维的单体是丙烯腈,它可由以下两种方法制备:
方法一:CaCO3![]() CaO
CaO![]() CaC2
CaC2![]() CH
CH![]() CH
CH![]() CH2=CH—CN
CH2=CH—CN
方法二:CH2=CH—CH3+NH3+![]() O3
O3![]() CH2=CH—CN+3H2O
CH2=CH—CN+3H2O
对以上两种方法的分析中,正确的是( )
①方法二比方法一步骤少,能源消耗低,成本低
②方法二比方法一原料丰富,工艺简单
③方法二比方法一减少了有毒气体的使用,减少了污染
④方法二比方一的反应需要温度高,耗能大
A. ①②③B. ①③④C. ②③④D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z均是中学化学中常见的物质,某同学用X、Y两种单质及Z的溶液进行实验,部分实验内容如下表所示:
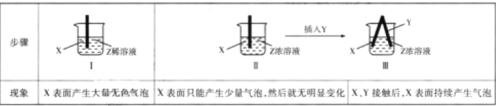
(1)I中反应物与生成物总能量的大小E(反应物)_____E(生成物)(填“ >”“< ”或“=”),仅仅由I、II中的信息可知,Z可能是_____。
(2)若X是铝,在温度不变时向I中分别加入(适量)等物质的量的NaCl、KCl、CsCl后,产生无色气泡的速率明显加快,导致这种变化最可能的原因是_________。
(3)若X是铝,II中反应产生的气泡有特殊颜色,则发生反应的离子方程式为_____;单质Y不可能是____(填字母)。
A 铅 B 石墨 C 镁 D 银
(4)若Ⅲ溶液最终变成蓝色,写出负极上电极反应式_______;变化过程中,参与正极上放电的离子是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表述正确的是
A.22.4LHCl溶于水制得1L盐酸时,其浓度为1 molL-1
B.1L0.3molL-1的CuCl2溶液中含有Cu2+和Cl-的总物质的量为0.9mol
C.在K2SO4和NaCl的中性混合水溶液中,如果c(Na+)=c(SO42-),则c(K+)=c(Cl-)
D.10℃时,100mLKCl饱和溶液蒸发掉5g水,冷却到10℃时,它仍为饱和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在托盘天平的两盘上,分别放有两个质量相同的烧杯,各盛有6 mol·L-1HCl 100 mL,使天平达到平衡。分别向两烧杯中加入不超过5 g 的镁和铝,若要使其充分反应后天平仍保持平衡,则加入的镁与铝的质量之比为( )
A. 1∶1 B. 24∶27 C. 12∶9 D. 32∶33
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】异丙苯(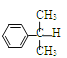 )氧化法是工业生产苯酚和丙酮最主要的方法。其反应和流程如下:
)氧化法是工业生产苯酚和丙酮最主要的方法。其反应和流程如下:
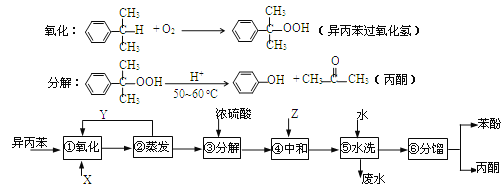
已知:
完成下列填空:
(1).X物质是 ;Y物质是 。
(2).浓硫酸的作用是 ,其优点是用量少,可能的缺点是 (写一条)。
(3).Z物质最适宜选择 (选填编号)。
a.NaOH b.Na2CO3c.NaHCO3d.CaCO3
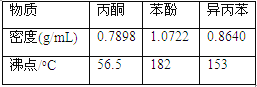
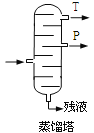
(4).步骤⑥分馏,工业上在分馏塔中进行,如右图,产品T是 ,请说明理由 。
废水中苯酚的含量,可根据苯酚与溴水的反应,用以下方法测定:
①把20.00mL废水、20mLKBrO3和KBr混合溶液[其中:
c(KBrO3)=0.0100mol/L,c(KBr)=0.0600mol/L]置于锥形瓶中,再加入10mL6mol/L的盐酸,迅速盖好盖子,摇动锥形瓶。
②充分反应后,稍松开瓶塞,从瓶塞和瓶壁间缝隙迅速加入10%KI溶液10mL(过量),迅速加盖,充分摇匀。加入少许淀粉溶液。
③用0.0250 mol/LNa2S2O3标准溶液滴定至终点。用去Na2S2O3溶液22.48mL。
(5).已知:BrO3–+5Br–+6H+→3Br2 + 3H2O ;写出苯酚与浓溴水反应的化学方程式 ;
第①步加盐酸、第②步加KI溶液,要迅速盖好盖子的原因是 。
(6).已知:I2+ 2Na2S2O3→2NaI + Na2S4O6;滴定终点的现象是 ;该废水中苯酚的浓度是 mol/L(保留4位小数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com