
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| 1 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 充电 |
| 放电 |
| ||
| 高温高压 |
| 时间/min | c(N2)/mol?L-1 | c(H2)/mol?L-1 | c(NH3)/mol?L-1 |
| 0 | 0.6 | 1.8 | 0 |
| 5 | 0.48 | X | 0.24 |
| 10 | 0.26 | 0.78 | 0.68 |
查看答案和解析>>
科目:高中化学 来源:湖南省永州八中2007届高三化学第三次月考试卷 题型:022
一定条件下,将W克的氢气或一氧化碳或是二者的混合气体,在足量的氧气中充分燃烧后,将生成的气体(水也是气体)通过足量的过氧化钠后,过氧化钠的质量增加W克,由些分析得出只要其化学组成符合________的物质,在足量的氧气中充分燃烧后,将生成的气体通过足量的过氧化钠时其增加质量就等于原来物质的质量.符合上述组成的某种有机物0.1mol在氧气中充分燃烧后生成CO2和H2O水均为0.2mol,并放出akJ热量,则在通常状态下该物质燃烧的热化学方程是________.符合上述组成的有机物可能的结构简式有________
查看答案和解析>>
科目:高中化学 来源:2013学年黑龙江省友谊县红兴隆管理局第一高级中学高一6月月考化学试卷(带解析) 题型:填空题
已知拆开1 mol氢气中的化学键需要消耗436 kJ能量,拆开1 mol氧气中的化学键需要消耗498 kJ 能量,根据图中的能量图,回答下列问题: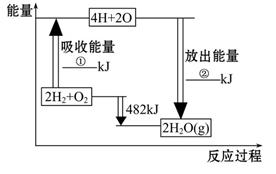
(1)分别写出①②的数值:
①___________KJ; ②____________KJ。
(2)生成H2O(g)中的1 mol H—O键放出_____________kJ的能量。
(3)已知:H2O(l)====H2O(g)
ΔH =" +44" kJ·mol-1,试写出2 mol氢气在足量氧气中完全燃烧生成液态水的热化学方程______________________。
查看答案和解析>>
科目:高中化学 来源:2013学年黑龙江省高一6月月考化学试卷(解析版) 题型:填空题
已知拆开1 mol氢气中的化学键需要消耗436 kJ能量,拆开1 mol氧气中的化学键需要消耗498 kJ 能量,根据图中的能量图,回答下列问题:

(1)分别写出①②的数值:
①___________KJ; ②____________KJ。
(2)生成H2O(g)中的1 mol H—O键放出_____________kJ的能量。
(3)已知:H2O(l)====H2O(g)
ΔH =" +44" kJ·mol-1,试写出2 mol氢气在足量氧气中完全燃烧生成液态水的热化学方程______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com