
| A、1.01×105 Pa、25℃时,2.24 L Cl2中含有的原子数为0.2×6.02×1023 |
| B、0.1L 3mol?L-1 NH4NO3溶液中含有的N原子数目为0.3×6.02×1023 |
| C、5.6g铁粉与足量CuSO4溶液反应生成的铜原子数为1×6.02×1023 |
| D、46g NO2和N2O4的混合物中含有的原子数为3×6.02×1023 |


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:
| A、标况下,铁在2.24 L Cl2中充分燃烧,恰好反应,转移的电子数为0.2NA |
| B、0.1 mol Na和氧气在一定条件下反应生成3.5 g 氧化物时,失去的电子数为0.1NA |
| C、含4 mol HCl的浓盐酸和足量的MnO2反应时,转移的电子数为2NA |
| D、常温常压下,28克N2和CO的混合气体所含的原子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O和Na2O2都是白色固体 |
| B、Na2CO3能与石灰水反应而NaHCO3不反应 |
| C、Na2CO3受热后稳定性比NaHCO3强 |
| D、Na2O和Na2O2都能与水反应生成O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、浮在乙醇面上,融化成闪亮的小球 |
| B、沉到乙醇底部,融化成闪亮的小球 |
| C、沉到乙醇底部,缓慢产生气泡,钠不融化 |
| D、浮在乙醇面上,钠不融化但四处游动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、HCl的电子式: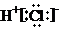 |
| B、C-12原子:12C |
| C、乙酸的结构简式:C2H4O2 |
| D、NH3?H2O的电离方程式:NH3?H2O→NH4++OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在80℃时,0.40mol的N2O4气体充入2L固定容积的密闭容器中发生如下反应:N2O4(g)?2NO2(g)△H>0,隔一段时间对该容器内的物质进行分析得到如下数据:
在80℃时,0.40mol的N2O4气体充入2L固定容积的密闭容器中发生如下反应:N2O4(g)?2NO2(g)△H>0,隔一段时间对该容器内的物质进行分析得到如下数据:| 时间(s) n(mol) |
0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com