

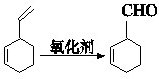
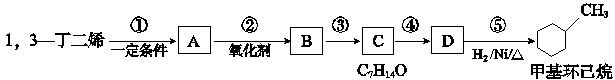
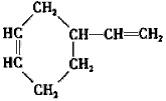

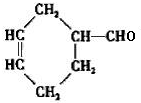

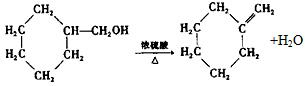


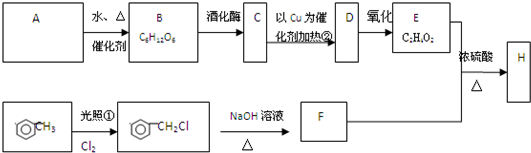
 ,结合A发生信息Ⅱ中反应生成B,B为
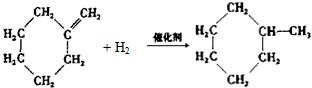
,结合A发生信息Ⅱ中反应生成B,B为 ,结合C的分子式可知,B与氢气发生全加成反应生成C,C为
,结合C的分子式可知,B与氢气发生全加成反应生成C,C为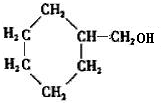 ,C发生消去反应生成D,D为
,C发生消去反应生成D,D为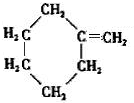 ,据此解答.
,据此解答. ,结合A发生信息Ⅱ中反应生成B,B为
,结合A发生信息Ⅱ中反应生成B,B为 ,结合C的分子式可知,B与氢气发生全加成反应生成C,C为
,结合C的分子式可知,B与氢气发生全加成反应生成C,C为 ,C发生消去反应生成D,D为
,C发生消去反应生成D,D为 ,
, ,B为
,B为 ,
, ;
; ;
; ,
, ,
, ;
; .
.

科目:高中化学 来源: 题型:
| △ |




查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
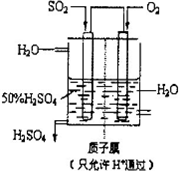 (2010?聊城模拟)利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.
(2010?聊城模拟)利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.| 1 |
| 2 |
| 10 |
| 3 |
c(C
| ||
c(S
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| +4 |
| Xe |
| +6 |
| Xe |
| +6 |
| Xe |
| c(H+)×c(F-) |
| c(HF) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com