
| 3 |
| 4 |
| 12n |
| 12n+2n |
| 12 |
| 44 |
| 2 |
| 18 |
| n(C) |
| n(H) |
| ||
|
| 9 |
| 20 |


科目:高中化学 来源: 题型:
| 选项 | 操作及现象 | 溶液 |
| A | 通入CO2,溶液变浑浊.再升高至65℃以上,溶液变澄清. | C6H5ONa溶液 |
| B | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失. | Na2SiO3溶液 |
| C | 通入CO2,溶液变浑浊.再加入品红溶液,红色褪去. | Ca(ClO)2溶液 |
| D | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失.再加入足量NaOH溶液,又变浑浊. | Ca(OH)2溶液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.24L |
| B、4.48L |
| C、6.72L |
| D、3.36L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、上述反应的热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-Q1 kJ |
| B、上述反应说明相同条件下,1 mol N2和3 mol H2 的总键能小于2 mol NH3的总键能 |
| C、相同条件下将2 mol N2和6 mol H2置于相同容器中充分反应后放出的热量为Q2kJ,Q2=2Q1 |
| D、氨水和NaOH中和反应的热化学方程式可表示为:H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ.mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 组别 | c(一元酸) | c(NaOH)/mol/L | 混合溶液的pH |
| 甲 | c(HX)=0.1mol/L | 0.1 | pH=a |
| 乙 | c(HY)=c1 mol/L | 0.1 | pH=7 |
| 丙 | c(HZ)=0.1mol/L | 0.1 | pH=9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度] | NaNO3 | KNO3 | NaCl | KCl |
| 10°C | 80.5 | 20.9 | 35.7 | 31.0 |
| 100°C | 175 | 246 | 39.1 | 56 |
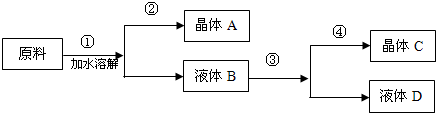
查看答案和解析>>
科目:高中化学 来源: 题型:
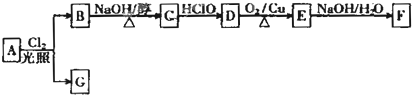
 :请回答下列问题:
:请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com